
1.下列描述属于物质化学性质的是 ( )
A.溶解性、稳定性 B.可燃性、氧化性
C.颜色、状态 D.溶点、沸点
32.某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物。因为Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O。
(1)该小组同学准确称取了8.0g黑色CuO粉末放人大试管中,不断通人足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为 。
(2)该小组在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g。此红色固体中氧元素的质量为 ,以此推得Cu2O的质量为 。
(3)将(2)中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:Cu2O+2HCl====CuCl2+Cu+H2O),充分搅拌,除有红色固体外,还发现溶液变蓝。试计算此蓝色溶液中CuCl2:的质量分数。
(3)比较三种猜想的异同,如果猜想②成立,设计实验,用两种方法加以证明。按相关要求填写下表。
|
|
实验操作 |
实验现象 |
|
方法一 |
|
|
|
方法二 |
|
|
31.学习了酸和碱的知识后,小松知道了白醋的主要成分是醋酸(CH3COOH)。为了测定白醋中醋酸的质量分数,他把4%的NaOH溶液滴加到30g白醋中,待反应恰好完全时(假定其他成分不参加反应),共用去NaOH溶液25g。
(1)已知反应的化学方程式为:CH3COOH+NaOH====CH3COONa+H2O,该反应的类型是 。
(2)请计算白醋中醋酸的质量分数。
30.某同学在实验结束进行废液处理时,将碳酸钠溶液、稀盐酸倒入到指定的洁净容器中,看到有气泡产生,待不再产生气泡时,又倒入了氢氧化钙溶液,发现该容器中有白色沉淀产生,这一现象引起了他的注意。为了解以上三种物质之间的反应情况,他决定从反应后溶液中的溶质进行探究。
(1)他对反应后溶液中的溶质组成作出了两种猜想(猜想①和猜想②)。请你再补充
一种猜想(猜想③)。
猜想①:溶质为氯化钠、氢氧化钠;
猜想②:溶质为氯化钠、氢氧化钠、氢氧化钙;
猜想③:溶质为 。
(2)比较三种猜想,说明该同学作出猜想①的理由:
(3)比较三种猜想的异同,如果猜想②成立,设计实验,用两种方法加以证明。按相关要求填写下表。
|
|
实验操作 |
实验现象 |
|
方法一 |
|
|
|
方法二 |
|
|
29.物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象。某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
方案一:先用pH试纸测定NaOH溶液的pH值,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH值,如果测得的pH值逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
(1)用pH试纸测定溶液的pH值时,正确的操作是: 。
(2)简述强调“测得的pH值小于7”的理由: 。
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了。该小组对这种意外现象的原因作了如下猜想:
①可能是酚酞溶液与空气中的氧气反应,使红色消失;
②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失。
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液。实验中“加热”和“滴入植物油”目的是 。实验结果表明酚酞溶液红色消失与空气中的氧气无关。
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3。溶液,在其中滴入
酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:
结论l:说明Na2CO3溶液呈 性;
结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关。
(3)该小组同学通过查阅资料得知:当氧氧化钠溶液浓度很大时,就会出现上述意外现象。请设计实验证明该方案中取用的NaOH溶液浓度过大:①实验方法 ,②观察到的现象 。
方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。该组同学将不同含量的盐酸和NaOH溶液各10 ml.混合,用温度计测定室温下混合前后温度的变化,并记录厂每次混合前后温度的升高值At(见下表)。
|
编号 |
盐酸 |
NaOH溶液 |
&/℃ |
|
1 |
3.65% |
2.00% |
3.5 |
|
2 |
3.65% |
4.O0% |
Z |
|
3 |
7.30% |
8.O0% |
14 |

(1)表中 。
。
(2)某同学在没使用温度计的情况下,通过如图l一8所示装置完成了实验。则该同学根据 判断NaOH溶液与稀盐酸发生了中和反应。
28.一位同学取了一瓶井水进行实验,请和他一起完成实验报告:
(1)用烧杯分别取少量井水和蒸馏水,加入适量 ,搅拌。发现蒸馏水中泡沫多、井水的泡沫少。结论:井水是硬水。
(2)另取井水加热煮沸,发现有难溶于水的固体生成。
(3)过滤,把得到的难溶固体置于试管中,加入过量的盐酸,现象是 ,并有气体产生;把生成的气体通入过量的澄清石灰水中,现象是 ,化学方程式是 。
结论:难溶物中含有碳酸盐。
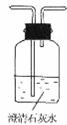
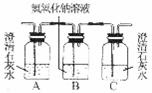
27.为缓解石油资源危机,近年来,我国正在大力推广使用“乙醇汽油”。乙醇不完全燃烧时的产物有CO、CO2、H2O。用下表中的仪器组装成一套完整的装置可检验这些产物。
|
编号 |
① |
② |
③ |
④ |
|
装置 |
 |
 |
 |
 |
(1)产物依次通过 (按从左至右顺序填装置编号)。
(2)实验过程中可观察到:装置②的A瓶中石灰水变浑浊,C瓶中石灰水不变浑浊。
A的作用是 。C的作用是 。
(3)装置④中盛放的药品是 ,装置①的作用是 。
(4)尾气的处理措施是 。
26.A、B、C三种可溶性化合物,分别由Fe3+、Na+、Cu2+、S042-、Cl-、OH-六种离子中的两种组成(离子不能重复选用)。取上述物质的稀溶液进行实验,现象如下:
B+C一红褐色沉淀 B+Ba(NO3)2-白色沉淀
根据以上事实推断:A是 ;B是 ;C是 。
25.有A、B两种固体物质,A是一种化肥,B广泛用作食品干燥剂。把A、B分别放入水中,前者所得溶液温度显著降低,后者与水反应生成C并放出大量热;将A与C的粉末混合、研磨,会嗅到刺鼻的氨味。
(1)A物质是 ,B物质是 。
(2)A物质属于化肥中的 肥(选填“氮”“磷”或“钾”)。
(3)指出C物质在农业生产中的一种用途: 。
(4)把A放入水中所得溶液温度显著降低的原因是 。
(5)B与水反应的化学方程式是 ,反应类型是 反应。
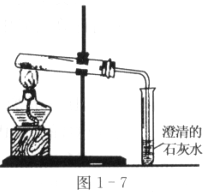
24.由C、CuO、Fe三种物质组成的混合物,放在试管中,如图17所示高温加热。当观察到澄清石灰水变浑浊时,停止加热,密封冷却至室温;然后往试管中加入稀硫酸,观察到有气泡冒出,且红色物质明显增加。请根据这些信息,推断红色物质产生和增加的可能的原因(用化学方程式表示):
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com