
26.氢氧化钠溶液暴露在空气中易生成碳酸钠而变质,反应的化学方程式是____________,如何判断氢氧化钠溶液是否变质?三位同学分别从酸、碱、盐中选择一种物质的溶液进行试验,都能达到判断的目的,请完成下表:
|
所选的试剂 |
反应现象 |
化学方程式 |
|
|
|
|
|
|
|
|
|
|
|
|
思考:能否用酚酞试液判断NaOH溶液是否变质?为什么____________________。
25.通过海水晒盐制得的粗盐中常含有Na2SO4、CaCl2和MgCl2等杂质,在食盐生产过程中需要将这些杂质除去,请回答:
在实验操作中,通常需要加入过量的除杂试剂,有一化学课外活动小组为了除去粗盐中的杂质,设计了下列实验步骤:
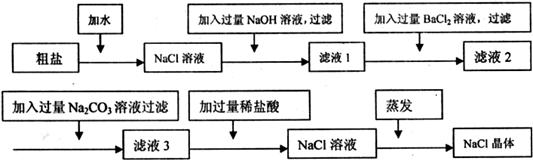
(1)加入过量氢氧化钠溶液反应化学方程式______________________________。
(2)加入过量氯化钡溶液反应化学方程式________________________________。
(3)加入过量碳酸钠溶液的目的________________________________________。
(4)加入过量盐酸的目的是____________________________________________。
(5)最后制得的氯化钠晶体中含有盐酸吗?为什么?____________________。
24.下图是甲、乙两固体物质的溶解度随温度变化的曲线图,据此我能回答下列问题:
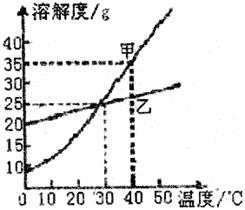
(1)40℃时,甲物质的溶解度为__________g。
(2)溶解度随温度变化影响比较大的物质是__________。
(3)30℃时,向100g水中加入30g乙物质,充分溶解后,所得溶液是(填“饱和”或“不饱和”)溶液,所得溶液中溶质的质量分数为__________。
23.一张洁白干燥的滤纸上,依次喷洒A、B、C三种无色液体。当喷洒A时,滤纸上无明显变化;再喷洒B时,滤纸上出现一只红色小猫(如下图);最后喷洒C时,小猫渐渐消失。回答下列问题:滤纸上的小猫可能是用_________画的。无色液体A是_________,B是__________,C是__________。

22.向氢氧化钠溶液中逐滴滴加稀盐酸,并用PH试纸监测其酸碱度。当PH=10时溶液中溶质为_________;当PH=7时溶质为_________;当PH=3时溶液中的溶质为_________。
21.有Na、O、S、H四种元素,按要求书写化学式:
酸__________ 碱__________ 盐__________
非金属氧化物__________ 金属氧化物__________
20.在茶缸和脸盆等铁制品表面烧制搪瓷的目的是
A.增大硬度防止撞坏 B.增大厚度防止磨损
C.防止铁生锈且美观 D.美观和杀菌消毒
19.将一瓶盐酸分成三等份,分别跟等质量的铝、铁、锌反应后,三种金属都有剩余,且剩余金属的质量为铝>铁>锌,如生成的H2质量分别为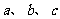 则其关系为
则其关系为
A.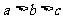 B.
B.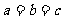 C.
C.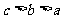 D.
D.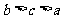
18.将铁片分别放入下列溶液中充分反应后,溶液质量比反应前减少的是
A.CuSO4溶液 B.H2SO4溶液 C.FeSO4溶液 D.HCl溶液
17.保护海洋环境所采取的下列措施中不正确的是
A.控制陆地污染,实行陆地污染物排放总量控制
B.禁止工业“三废”的排放
C.可以使用含磷洗衣粉,以增加海水中的磷,从而有利于海生植物的生长
D.推广使用对环境危害较小的农药、化肥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com