
35.(5分)一化学兴趣小组对某生铁样品中铁的质量分数进行探究.请按要求完成下列探究报告.
[实验目的]
测定某生铁样品中单质铁的质量分数.
[资料支撑]
生铁中除铁外,还含有碳、硅、锰、磷和硫等元素.
碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);
硅、锰、磷、硫存在形式较为复杂;这些物质通常都不与稀硫酸发生化学反应.
[实验方案]
生铁样品与过量的稀硫酸反应,测定反应前后可称量物质的质量差.
[实验过程]
(1)取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g;
(2)向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入少量稀硫酸以确保过量,测得共用去稀硫酸247.3g;
(3)静置,称量.称得烧杯和剩余物质的总质量为348.7g.
[数据处理]计算该生铁样品中单质铁的质量分数是多少?(写出计算过程)
________________
[交流讨论]
(1)实验称量时称量物应放在托盘天平的 盘(选填“左”或“右”);
(2)实验过程中稀硫酸要过量的原因是 ;
(3)经质检部门精确测定,该样品中铁元素的总含量为95.2%.假设没有与硫酸反应的铁都以Fe3C形式存在,则样品中Fe3C的质量分数为 .
34.(4分)某石灰厂有一批石灰石原料,为了测定该石灰石的纯度,厂化验室技术员称取6.25g研碎的石灰石粉末,进行四次高温煅烧(杂质没有变化)、冷却、称量剩余固体质量的重复操作,记录数据如下:
|
操作次序 |
第一次 |
第二次 |
第三次 |
第四次 |
|
剩余固体质量 |
5.55g |
4.35g |
4.05g |
4.05g |
试计算:
(1)完全反应后生成二氧化碳 g; (2)石灰石样品中碳酸钙的质量分数;
(3)充分煅烧20t这种石灰石,可制得含杂质的生石灰的质量.
33.(3分)20℃时NaNO3的溶解度是88g.将50gNaNO3放入50g水中,充分溶解后,形成20℃时NaNO3的 (选填“饱和”或“不饱和”),该溶液的质量是 g,此时溶液中NaNO3的质量分数等于 %.
32.(2分)2008年5月12日四川汶川大地震后,为了预防疫情,防疫人员使用了各种消毒
剂对环境进行消毒.亚氯酸钠(NaClO2)是一种重要的消毒剂.试计算:
(1)亚氯酸钠中Na、Cl、O三种元素的质量之比为 .
(2)现要配制质量分数为16%的亚氯酸钠消毒液1500kg,需要亚氯酸钠
31.(9分)“嫦娥一号”卫星发射成功,标志月球探测成为中国航天的现实.
(1)“嫦娥一号”使用的燃料是液氢,助燃剂是液氧.氧气从淡蓝色液体变成无色气体发生了 变化,氢气燃烧的化学方程式为 .液态氢作燃料除燃烧时产生较大的推动力外,另一个优点是 .对于目前全世界出现能源危机,以及燃烧对环境的影响,我们应该合理开发利用的新能源有(至少填两种)
(2)月球上的3He(3表示相对原子质量)蕴藏量巨大,探月的目标之一是探测核聚变燃料3He的分布.地球上的氦元素主要以4He形式存在.从原子的构成来看,3He、4He两种原子的 数不同,化学性质 .
(3)“嫦娥一号”另一个目标是探测下列14种元素的含量和分布:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆).其中属于金属元素的有 种.
(4)月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”.我国四川省有大型钒钛磁铁矿,由钒钛磁铁矿提取金属钛的主要工艺过程如下:
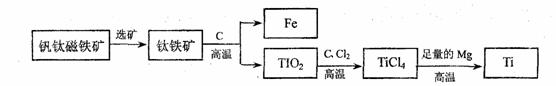
①钛铁矿的主要成分是FeTiO3 (钛酸亚铁),其中钛的化合价为 价.
②上述生产过程中得到的金属钛中混有少量金属杂质,可加入 除去.
30.(4分)下图表示某些物质间转化关系(反应条件和部分产物已省略).其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属.

请回答下列问题:
(1)反应①中A物质的作用是 ;
(2)反应④的化学方程式: ;
(3)在日常生活中为防止反应②的发生,可采取的措施是 (写一点即可);
(4)在自然界中普遍存在反应⑤,其名称为 .
29.(3分)(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以a 计分)
a.国家“西气东输”工程使得东部沿海地区广大居民用上天然气(主要成分甲烷)作燃料.
已知1kg甲烷燃烧生成液态水和二氧化碳,放出的热量约为5.87×107J.试填空.
(1)参加上述反应的氧气和生我的二氧化碳的化学计量数之比v(O2):v(CO2)= ;
(2)若1kg甲烷燃烧生成气态水和二氧化碳放出的热量 5.57×107J(选填“>”或“<”或“=”);
(3)16kg甲烷燃烧生成水和二氧化碳,至少消耗氧气的质量为 kg.
b.乙醇是一种清洁能源.乙醇的燃烧可发生以下两个反应:
①C2H6O+3O2 2CO2+3H2O
2CO2+3H2O
②aC2H6O+5O2 2CO2+2CO+6H2O
2CO2+2CO+6H2O
试填空.
(1)反应②中的化学计量数a= ;
(2)反应 (选填化学方程式的序号)属于完全燃烧,产物无毒性.
(3)9.2g乙醇在空气中若按化学方程式②发生反应,生成一氧化碳的质量为 g.
28.(3分)下列实验操作中的先后顺序正确的是 (选填合理选项的字母序号,答案并非唯一).
A.加热碱式碳酸铜检验气体产物,结束时先将导管从石灰水中移出,再熄灭酒精灯
B.检查气密性时.先旋紧连导管的单孔橡皮塞,将导管插入水中,再用手握住试管
C.用启普发生器制氧气时.先向容器内添加锌粒,再向球形漏斗内注入适量稀硫酸
D.制取氧气时,先将导管伸入倒置于水槽中的集气瓶口.再加热盛高锰酸钾的试管
27.(10)利用下列仪器进行气体的制取和性质实验.请完成下列问题.

其中E是双孔橡皮塞
(1)仪器B、I的名称分别是 、 ;
(2)实验室用高锰酸钾制取氧气,仪器的装置组合是 (填字母),反应的化学方程式为 .
(3)实验室制取二氧化碳,所用的药品是 ,从上述仪 器中组合3套发生装置为 、 、 (填字母),检验二氧化碳收集满的方法是 .
(4)在B中收集满二氧化碳,倒扣于盛有水的H中,一段时间后,B中液面 、(填“上升”或“不变”);若B中充满下列 气体,也会发生类似现象.
A.H2 B.NO2 C.HCl D.CO
(提示:①3NO2+H2O===2HNO3+NO,NO气体难溶于水;
②同温同压下,任何气体体积之比等于分子数之比.)
26.(3分)已知有如下反应:A+B→C+D.(答题时需注明必要的反应条件)
(1)A为CO2、B为H2O,则该反应(该反应的生成物之一是有机物葡萄糖,化学式为(C6H12O6)的化学方程式是 .
(2)若A为A1、B为ZnSO4 (溶液),C、D的化学式分别是 、
(3)若反应为A+2NaOH=C+Cu(OH)2↓,则A和C的相对分子质量之差为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com