
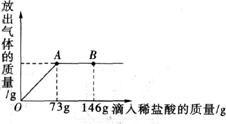
26.(5分)在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加足量水溶解,制成溶液。向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:
请根据题意回答问题:
(1)当滴加了73g稀盐酸时,放出气体的总质量为__________g。
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式)_______________。
(3)当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
25.(分)四川汶川抗震救灾期间,为防止灾后疫情的发生,每天需要喷洒大量消毒液。欲配制800kg溶质质量分数为0.5%的过氧乙酸消毒液,需用溶质质量分数为16%的过氧乙酸溶液的质量为_________kg。
24.(分)请你参与某学习小组进行研究性学习的过程,并协助完成相关任务。
[研究课题]探究热水壶底部水垢的主要成分
[查阅资料]该小组同学通过查阅资料知道,天然水中一般都含Ca2+、Mg2+、HCO 等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐、碱等的混合物),同时,他们还查阅到下列有关物质的溶解性:
等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐、碱等的混合物),同时,他们还查阅到下列有关物质的溶解性:
|
物质 |
Ca(HCO3)2 |
Mg(HCO3)2 |
Ca(OH)2 |
Mg(OH)2 |
CaCO3 |
MgCO3 |
|
溶解性 |
可溶 |
可溶 |
微溶 |
不溶 |
不溶 |
微溶 |
[提出猜测]水垢的主要成分一定含有Mg(OH)2和_______,可能含有Ca(OH)2_______。
[设计方案](1)维靖同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入__________________,没有白色沉淀,说明水垢中无Ca(OH)2。
(3)林硕同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分,其主要实验步骤如下:
①按图组装仪器,将50g水垢试样放入锥形瓶中,加入足量某酸溶液;
②测量一定时间内干燥管内物质增加的质量(见下列曲线);
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变。


讨论:
a.步骤①加入样品前还应检查____________________,所加的酸溶液是____________;
b.装置Ⅱ的作用是_____________________________;从导管A处缓缓鼓入一定量的空气时,装置Ⅰ的作用是_______________________________________________________;
c.研究性小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是___________。
[实验结论]通过上述研究可知:水垢的主要成分有____________________。
23.(5分)某校化学兴趣小组的同学为了探究裹在皮蛋壳外固体的成分,从资料和网上到腌制皮蛋的原料和方法。将生石灰、纯碱、草木灰(主要成分K2CO3)、食盐等用水调成糊状,敷于蛋上,密封保存,下面请你参与他们的讨论并协助完成相关实验。
(1)向烧杯中加入研碎的皮蛋外壳固体,再加入适量的水,搅拌后静置,观察烧杯底部有白色固体,该白色固体中一定含有_____________________;烧杯的上层溶液中一定含有__________________________________;
(2)为研究烧杯内的溶液中还可能含有的物质,同学们继续进行探究。
①志鹏同学从烧杯中取出少量溶液,加入稀盐酸,观察到有气泡冒出,说明溶液中含有________________;
②久馨同学从烧杯中取出少量溶液,向其中滴入酚酞试液,溶液变红。你认为该溶液中使酚酞试液变红的物质应该有__________、_________;
22.(2分)A是一种白色难溶于水的钙盐,由三种元素组成,其相对分子质量为100。

(1)写出A与盐酸反应的化学方程式:_______________________________________;
(2)D中含有的溶质可能有哪几种情况?
__________________________________________________________________________。
21.(3分)某课外小组的同学们收集了含一氧化碳和二氧化碳的废气,为了确认这种废气的组成,他们在实验室按如下装置进行了实验。

(1)B装置中盛放足量浓氢氧化钠溶液,其作用是_______________________________;
(2)C装置中发生反应的化学方程式是__________________________;
(3)A装置和D装置完全相同,其作用的不同之处是_____________________________。
20.(9分)根据下列实验装置图回答问题:

(1)请写出标号仪器的名称:①__________,②___________;
(2)若使用高锰酸钾固体制取氧气,应选择的发生装置为________________,收集装置为__________(填字母),反应的化学方程式为___________________________________;
(3)装置B可用于制备的气体有_____________(答两种);
(4)实验室在制取二氧化碳气体时常混有水蒸汽和氯化氢气体,如果用装置F来除去水蒸汽,气体应从导管__________端进入,可选用_________做干燥剂。如果用装置F来检验氯化氢气体,F中应盛放的试剂是_____________。
19.(3分)下图是元素周期表中的一部分。
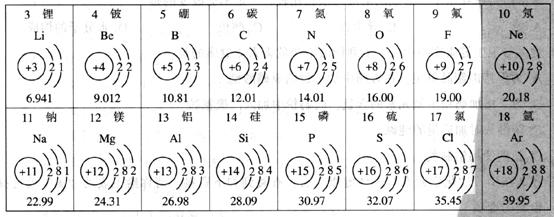
根据上图所示内容,回答下列问题。
(1)对上图所示内容说法正确的是____________;
①原子序数为14的元素是金属元素
②原子序数为15的磷原子相对原子质量为30
③氖和氩的原子核外电子排布都属于稳定结构
④从核外电子排布看钠原子容易失去电子
(2)表中不同元素最本质的区别是________________;
①质子数不同 ②中子数不同
③相对原子质量不同 ④核外电子数不同
(3)从上图中我们发现:随着原子序数的递增,其原子结构(或元素的性质)呈现的变化具有一定的规律。下面是天逸同学在学习时寻找出图中的一些变化规律,其中正确的是____________________。(填a、b、…)
①从上图的横向看: a.随着原子序数的递增,原子最外层电子数从1递增到8
b.每一横行中元素原子的核外电子层数相同
②从上图的纵向看: c.每一纵行中不同元素的原子最外层电子数相等
③从其他变化规律看: d.金属元素的原子最外层电子数一般少于4个
18.研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
[假设]H2O2生成O2的快慢与催化剂种类有关。
[实验方案]常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间。
[进行实验]下图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是____________,其理由是______________________________________________________。

[实验记录]
|
实验编号 |
1 |
2 |
|
反应物 |
6%H2O2 |
6%H2O2 |
|
催化剂 |
1 g红砖粉 |
1 g MnO2 |
|
时间 |
152
s |
35
s |
[结论]该探究过程得出的结论是__________________________________________。
17.研究表明:木糖醇是一种理想的蔗糖替代品。它具有甜味足、溶解性好、防龋齿、适合糖尿病患者食用的优点。下图是木糖醇和蔗糖的溶解度曲线。请回答下列问题:

(1)在人体体温37℃时,两种物质的溶解度:木糖醇_______蔗糖(填“<”或“>”或“=”)。
(2)40℃时,将50g木糖醇放入50g水中,充分溶解后所得溶液的质量为_________g;
(3)现有60℃时木糖醇和蔗糖的两种饱和溶液,欲使它们溶质的质量分数相等,且仍为饱和溶液,可采取的一种方法是___________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com