
33.(8分)为探究CO2的化学性质,需要制取并收集干燥的CO2,以下是老师提供的一些实验装置。
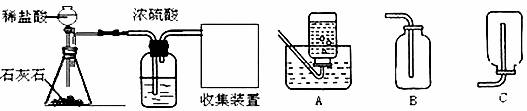
(1)实验室制取CO2的化学方程式为 ,浓硫酸的作用是 ,收集装置为 (填字母)。
(2)化学课上,李芹同学将燃烧的钠迅速伸入盛有CO2的集气瓶中,钠在集气瓶中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
[提出问题]黑色颗粒和白色物质可能是什么呢?
[进行猜想]你认为黑色颗粒是_____________,小明认为白色物质是氧化钠,小艺认为是碳酸钠,小亮认为是氧化钠和碳酸钠的混合物,小华认为是氢氧化钠。
李芹同学认为小华的猜想是错误的,其理由是__________________。
[查阅资料]CaCl2+Na2CO3=CaCO3↓+2NaCl ,氧化钠为白色粉末,溶于水生成氢氧化钠。
[实验探究]李芹同学对白色物质进行实验探究。
实验方案1:取该样品少量于试管里,加适量水,振荡,样品全部溶于水。向其中加入无色酚酞试液,观察到溶液变成红色。结论:白色物质为氧化钠。
实验方案2:取该样品少量于试管里,加适量水,振荡,样品全部溶于水。向其中加入过量的CaCl2溶液,出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现。结论:白色物质为____________________。
[反思评价]小娟同学认为实验方案1得出的结论不正确,其理由是_____________。
[得出结论]钠在二氧化碳中燃烧的化学方程式为_____________。
32.(5分)在化学的学习中,同学们知道:聚乙烯塑料只含C、H两种元素,如用焚烧方法处理废弃塑料会造成大气污染。化学兴趣小组对聚乙烯塑料在空气中燃烧生成的碳的氧化物的组成进行探究。
[提出猜想]A.只有CO2 ; B.只有CO ; C.既有CO2,也有CO
[查阅资料]微量CO遇到浸有磷钼酸溶液的氯化钯黄色试纸,试纸立即变蓝;而CO2遇该试纸,试纸不变色。
[设计方案]化学兴趣小组在老师的指导下,设计下图所示实验,通过观察装置B、装置C的实验现象,验证猜想。
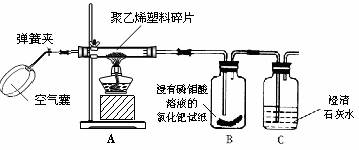
[实验探究]请你帮助他们写成实验报告。
|
实验步骤 |
实验现象 |
实验结论及化学方程式 |
|
点燃酒精灯加热,随即打开弹簧夹,通入干燥的空气。 观察装置B、装置C中的现象 |
装置B中的现象是: 装置C中的现象是: |
聚乙烯塑料在空气中燃烧,生成碳的氧化物中,既有CO2,也有CO。 装置C中反应的化学方程式为: |
[讨论]
(1)根据实验结论,从环保角度考虑,实验中应对尾气进行处理。处理方法是 。
(2)聚乙烯塑料在空气中燃烧,生成物中除了CO2、CO外,还应有的物质是 。
31.(6分)实验室常用下列装置来制取氧气:
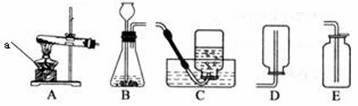
(1)写出图中有标号仪器的名称:a 。
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是 (填序号)。
(3)用高锰酸钾制取氧气时,发生反应的化学方程式为 ,基本反应类型为 。用E装置收集氧气的依据是 ,检验氧气是否集满的方法是 。
30.(6分) A-H是初中化学常见的8种物质,下图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应)。A、G都是单质,气体C常用于灭火,H中不含氧元素。请你回答:

(1)C的化学式为 ,H的名称是 ;
(2)写出标号①、②、③、④的化学方程式:
① ② ③ ④
29.(6分)溶液与人们的生活息息相关,而水是一种最常用的溶剂。
(1)保持水的化学性质的最小粒子是 。
(2)小明要净化收集的雨水,自制了一个简易净水器(如下图①所示),其中小卵石、石英沙和膨松棉的作用是 。
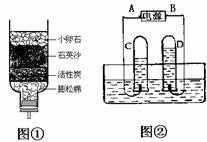
(3)上图②中A连接电源的____(填“正极”或“负极”)。该反应的化学方程式为 。该实验说明水是由 组成的。
(4)将75克20%的NaCl溶液稀释成15%的NaCl溶液,需要加水 mL(水的密度为1g/cm3)。
28.(6分)
(1)写出防止铁制品锈蚀的一种方法 。
(2)铁在氧气里燃烧的产物为 。
(3)写出一氧化碳与氧化铁反应的化学方程式 ,下图中酒精灯的作用是 。

(4)小明将某食品包装袋内的抗氧化剂撕开后发现,袋内有板结的铁锈。他推测该抗氧化剂的有效成分是 ,它的作用是 。
27.(6分)元素周期表和原子结构示意图是学习和研究化学的重要工具。请根据以下示意图回答问题。
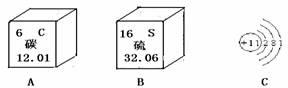
(1)根据A图可查出该原子的相对原子质量为 ,根据B图可判断该元素原子的质子数为 ,根据C图可判断该元素原子的最外层电子数为 ;
(2)上述三个图表示的三种元素最本质的区别是 ;
(3)请从Na、C、H、O、S五种元素中选择适当的元素,写出符合下列要求的物质的化学式:可以去除油脂的碱是 ,能除铁锈的酸是 。
26.(6分)
(1)豆浆机由于快捷方便而进入千家万户。请据下图所示回答:
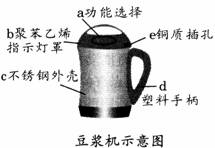
①制作材料中属于合成有机高分子材料的是 。(填字母)
②用金属材料制作电源插头的插孔,是利用了金属的 性。
(2)豆浆已成为众多家庭的早餐必备饮品,下表是豆浆中一些成分的平均质量分数:
|
成分 |
水 |
蛋白质 |
脂肪 |
糖类 |
钙 |
磷 |
铁 |
维生素A |
|
质量分数(%) |
96.0 |
1.8 |
0.7 |
1.1 |
0.01 |
0.03 |
0.0005 |
0.015 |
①豆浆中能为人体提供能量的营养素是 ,缺少表中 元素会引起贫血。
②若成年人每天饮用250 mL的豆浆(密度以1g/mL计算),则摄入钙的质量为
(3)生活中下列说法正确的是 。
A.食用豆浆可补充蛋白质 B.用霉变的大豆制作豆浆 C.食用豆浆可预防骨质疏松
25.有一Fe和FeO的混合物,测得其中铁元素的质量分数为80%。取该混合物7.0g,加足量稀硫酸完全溶解,生成硫酸亚铁的质量为
A.7.6g B.15.2g C.20.0g D.40.0g
24.为验证Fe、Cu、Ag三种金属的活动性是依次减弱的,某化学兴趣小组设计了如下图所示的四个实验。其中不必进行的是

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com