
3.我国盛产的八角茴香中存在莽草酸(C7H10O5)。由它合成的“达菲” (C16H31O8N2P)是是抗H1N1流感的一种药物。下列说法错误的是
A.莽草酸由三种元素组成 B.莽草酸的相对分子质量为174
C.用莽草酸合成达菲需要含氮的物质 D.由莽草酸合成达菲是物理变化
2.防止金属锈蚀是保护金属资源的有效途径,锌铬黄(化学式位ZnCrO4)常用于制防锈涂料。锌铬黄中铬元素的化合价为
A.+1 B.+2 C.+6 D.+7
1.下列一些物质的自我介绍,其中介绍自己化学性质的是

A.我是紫红色固体 B.我在天然界中硬度最大 C.我在常温下是气体 D.我会生锈
38.(8分)硝酸铵是农业生产中常用的化学肥料。为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取 2.0 g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液。发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O。反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如下图所示:
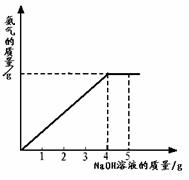
完成有关计算:
(1)NH4NO3中各元素的质量比为(H:N:O) ;
(2)样品中硝酸铵的质量分数;
(3)所得溶液中NaNO3的质量分数(保留两位小数)。
37.(6分)下图是“△△牌发酵粉”的部分信息,课外化学兴趣小组的同学对其进行了如下探究(请你完成相应填空):

[查阅资料]
(1)酒石酸是一种易溶解于水的固体有机酸;
(2)发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致;
(3)Na2CO 3受热不分解。
[提出问题]
NaHCO3在发酵粉加水或加热时如何产生CO2?
[猜 想]
甲.……
乙.酒石酸与NaHCO3在溶液中反应产生CO2
丙.NaHCO3加热产生CO2
[实验探究]
(1)小明同学取少量NaHCO3粉末于试管中,加入适量水,无气体产生,从而否定了猜想甲,则猜想甲是 。小明又将酒石酸溶液和NaHCO3溶液混合,产生了CO2,从而验证了猜想乙,说明了NaHCO3具有的性质之一是 ;
(2)小英同学为探究猜想丙设计了下图所示的实验装置:
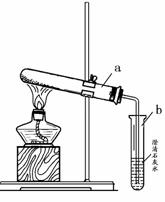
小英另取适量NaHCO3粉末加入a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊。b试管中反应的化学方程式为 。
持续加热直至两支试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末,向该粉末中滴加稀盐酸,有CO2产生,说明该粉末是 。
[小 结]
NaHCO3在发酵粉中产生CO2的条件是 ;
NaHCO3受热发生变化的化学方程式为 ;
36.(5分)实验是学习化学的一个重要途径。请从下列仪器中选用适当仪器用H2O2与MnO2制取并收集O2。

(1)仪器e的名称是 ;
(2)若用排空气法收集O2,产生并收集气体应该选用的仪器有(填代号) ,装入药品前必须进行的一步操作是 ;
(3)反应的化学方程式为 ;
(4)检验O2是否已经集满的方法是 。
34.(3分)如图所示,A、B、C、D、E、F均是初中化学常见物质。A与B发生的是复分解反应,B与C发生的是中和反应,F是人体正常生理活动必不可少的一种盐。结合图中信息,回答有关问题:

(1)E的化学式为 ;
(2)A与B反应的化学方程式为 ;
(3)C与D反应的化学方程式为 ;
33.(4分)元素周期律是学习和研究化学的重要工具。下表是元素周期表的部分信息:
|
1H 氢 |
1H 氢 |
2He 氦 |
||||||
|
3Li 锂 |
4Be 铍 |
|
5B 硼 |
6C 碳 |
7N 氮 |
8O 氧 |
9F 氟 |
10Ne 氖 |
|
11Na 钠 |
12Mg 镁 |
|
13A1 铝 |
14Si 硅 |
15P 磷 |
16S 硫 |
17C1 氯 |
18Ar 氩 |
|
19K 钾 |
20Ca 钙 |
…… |
|
|
|
|
|
|
认真分析信息,回答:
(1)地壳中含量最多的金属元素的符号是 ;
(2) 表示的是(填名称)
;
表示的是(填名称)
;
(3)由2、8、12号元素组成化合物的化学式 .
(4)上表中每一周期元素原子序数的变化规律是 。
32.(2分)写出下列变化的原因:
(1)墙内开花,墙外可嗅到花香是因为 ;
(2)硫酸、盐酸等酸类物质具有一些相似的化学性质,是因为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com