
1.下列物质的用途与其化学性质相关的是 ( )
A.铜作导线 B.煤炭作燃料 C.铁制炊具 D.黄金压成金箔
35.(3分)某小组同学将530 g碳酸钠溶液加入到280 g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%,计算加入的碳酸钠溶液中溶质的质量分数。
友情提示: 34、35题均要求写出计算过程。
34.(3分)钛(Ti)和钛合金被认为是21世纪的重要金属材料。钛可通过如下反应制得:
TiCl4+2Mg Ti + 2MgCl2,若要制得24 g 钛,需要镁的质量是多少克?
Ti + 2MgCl2,若要制得24 g 钛,需要镁的质量是多少克?
33.(8分)某校化学小组同学从家中带来食盐、水垢、纯碱、淀粉和洗衣粉5种物质。老师从中取出3种固体,研磨混合均匀(如下图所示),让同学们检验其成分。他们在查阅资料后,用5种已知物的性质实验作参照,探究未知粉末的成分。

(1)小组同学用5种已知物做性质实验。每次取样方法如下图所示:
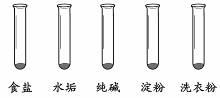
5种已知物的实验记录:
|
实验过程 |
部分实验现象 |
|
实验1:加水溶解 取样,分别加入足量的水充分溶解 |
淀粉、水垢:均有白色浑浊,试管底部有不溶物 洗衣粉:溶解,有洗涤剂泡沫浮于液面 |
|
实验2:加酚酞溶液 向实验1所得液体中分别滴入 2滴无色酚酞溶液 |
洗衣粉、纯碱:液体呈红色 其余物质:均无明显变化 |
|
实验3:加稀盐酸 另取样品,分别加入2 mL稀盐酸 |
洗衣粉:有洗涤剂泡沫浮于液面 水垢:有大量气体逸出 食盐、淀粉:均无气体产生 |
|
实验4:加碘水 另取样品,分别滴入2 滴碘水 |
淀粉:变蓝 其余物质:均不变蓝 |
根据上述实验记录回答:
①该洗衣粉溶液pH_____7 (填“>” 、“<”或“=”);
②写出纯碱与稀盐酸反应的化学方程式______________。
(2)小组同学用未知粉末重复上述实验进行成分探究。
未知粉末的实验记录:
|
|
实验1 加水溶解 |
实验2 加酚酞溶液 |
实验3 加稀盐酸 |
实验4 加碘水 |
|
未知粉末 实验现象 |
白色浑浊,试管底部有不溶物,有洗涤剂泡沫浮于液面 |
液体呈红色 |
有大量气体逸出 |
变蓝 |
参照5种已知物的性质实验,分析未知粉末的成分:
未知粉末中一定含有的两种物质是_______和_______,还含有的第三种物质是_____或_________,请你设计检验这种物质的实验方案_________。
32.(5分)小刚和小丽两位同学用下图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应。

(1)小刚关闭K,通入二氧化碳 ,A、B中均无明显变化。B中盛放_____溶液。
(2)小刚打开K,继续通入二氧化碳。B中反应的化学方程式为__________。
此步实验目的是_______________。
小丽认为:通常状况下,1体积的水约能溶解1体积二氧化碳,因此上述实验不足以证明二氧化碳和氢氧化钠发生了反应。
(3)小丽用洗涤干净的上述装置重新实验,分别量取50 mL上述溶液放入A、B中,关闭K,通入约500 mL二氧化碳,A、B中均无明显变化。此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是____________________。
31.(6分)实验室制取气体所需装置如下图所示。

A B C D E
请回答以下问题:
(1)装置中标“a”的仪器名称是___________。
(2)用高锰酸钾制取氧气时,所选用的发生装置是________(填字母序号,下同),收集装置是C或___________。
(3)用大理石与稀盐酸制取二氧化碳时,所选用的发生装置是_____________,其反应的化学方程式为______________________。该装置还可用于制氧气,其反应的化学方程式为____________。
30.(7分)甲是初中化学中的常见物质,请根据下列叙述回答问题。
(1)若甲能与稀硫酸反应生成一种在标准状况下密度最小的气体,该化学式为____________,甲在常见的金属活动顺序中的位置是____________。
(2)若甲是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,则甲的化学式为_____。
(3)若甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,且X与Y能反应,则甲的化学式可能是_____________(写出一种即可),X与Y反应的化学方程式为_____________。
(4)若甲既能与水反应,将少量甲加到饱和石灰水中,溶液变浑浊,则下列说法正确的是_________(填字母序号)。
A.甲一定是二氧化碳
B.反应后溶质的质量一定减小
C.反应前后溶剂的质量保持不变
D.反应前后溶液中溶质的质量分数可能不变
29.(6分)铜和铁是生产、生活中广泛使用的金属。
(1)工业上用一氧化碳和赤铁矿(主要成分是氧化铁)冶炼铁,反应的化学方程式为
__________________________________。
(2)铁生锈的条件是_____________;铜表面也容易生成绿色铜锈,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3,其组成元素有________种。
(3)老师用生锈的铜片、铁粉和稀硫酸进行实验,实验过程如下图所示(部分生成物已略去)。
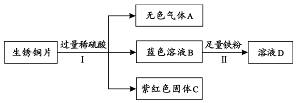
①紫红色固体C的化学式为________;
②写出II中反应的化学方程式_________________。
28.(6分)在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。

请回答以下问题:
(1)1个B分子中含有________个原子。
(2)A中氮元素和氢元素的质量比为___________。
(3)4种物质中,属于化合物的是___________(填图中字母)。
(4)该反应的基本反应类型为_________________。
(5)在该反应中,生成C和D的质量比为________(计算结果用最简整数比表示)。
27.(6分)随着经济的发展,能源与环境成为人们日益关注的问题。
(1)煤、__________和__________常称为化石燃料。
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是_______________。
(3)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体。为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷。该反应的化学方程式为______________。
(4)“绿色化学”的特点之一是“零排放”。一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物。其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是_______(填字母序号,下同)。
A.甲醇(CH4O) B.甲酸(CH2O2) C.乙醇(C2H6O) D.乙酸(C2H4O2)
(5)下列措施中,有利于降低大气中二氧化碳含量的是_____。
A.大量使用化石燃料
B.植树造林,增大植被面积
C.将二氧化碳变废为宝,循环利用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com