

3.日常生活中我们常接触到许多含氮的物质,如:N2、N2O、NH3、NO、N5O5、N2O4、NaNO2、NH4NO3,则这八种物质中氮元素显示的化合价共有 ( )
A.9种 B.8种 C.7种 D.6种
2.分类是学习和研究化学物质及其变化的一种常用的基本方法,家中常用的纯碱与下列哪组属于同一类物质 ( )
A.氨水、烧碱 B.盐酸、硫酸
C.二氧化硫、二氧化碳 D.氯化钠、硫酸铜
1.决定元素相对原子质量大小的主要因素是 ( )
A.核电荷数和电子数 B.质子数和电子数
C.质子数和中子数 D.中子数和电子数
21.某化学兴趣小组为了测定黄铜(铜锌合金)样品中铜的质量分数,他们取10g这种样品,把40g稀硫酸分四次加入到样品中,实验数据如下:
|
实验次数 |
稀硫酸的用量 |
剩余固体的质量 |
|
1 |
10
g |
8.70
g |
|
2 |
10
g |
7.40
g |
|
3 |
10
g |
6.75
g |
|
4 |
10
g |
6.75
g |
(1)从表中数据分析可知,第________次实验,样品中的锌完全反应;
(2)该黄铜样品中铜的质量分数为________
(3)求所用稀硫酸的溶质质量分数。
20.一次实验课上,细心的小红、小敏同学同时发现盛NaOH溶液的试剂瓶塞外有少量白色粉末。
[提出问题]白色粉末是什么呢?
[猜想与假设]①白色粉末是NaOH固体
②白色粉末是Na2CO3固体
③白色粉末是NaOH和Na2CO3的固体混合物
[实验探究]为了探究上述猜想,小红、小敏取白色粉末置于烧杯中,加入水配制成溶液。
(1)能否向溶液中滴加酚酞试液来证明上述猜想________(填“能”或“不能”),你的理由是________________________________________。
(2)小红取溶液少量于试管中,加入稀盐酸,有气泡产生,该实验说明猜想________不成立。
(3)为了探究另两个猜想哪个成立,小敏取溶液少量于试管中,加入足量CaCl2溶液,过滤。在滤液中滴加酚酞试液变红,表明猜想________成立。
[总结交流](1)小敏能否用Ca(OH)2代替CaCl2进行实验________ (填“能”或“不能”)。
(2)用化学方程式解释NaOH变质的原因________________________,该事实说明NaOH溶液或固体都必须密封保存。
19.一包白色固体粉末,可能由氯化钠、硫酸铜、硫酸钠、氯化钡、碳酸钙中的一种或几种组成,为证明其成分,做如下实验.
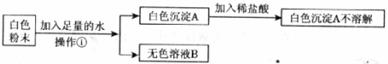
(1)操作①是_______。
(2)该白色粉末中一定没有_______ (填化学式.下同),可能含有_______。
(3)写出生成白色沉淀A的化学方程式_______。
(4)无色溶液B中一定含有的溶质是_______ (填化学式)。
18.下图是化学实验中制取H2、O2、CO2常用的几种装置。
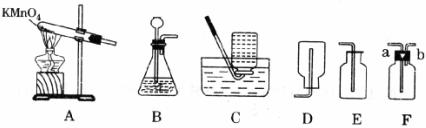
(1)实验室用高锰酸钾制取氧气应选用的气体发生装置是_______(填序号),该反应的化学方程式是_______,某同学用排水法收集氧气时,看到水槽中的水变红了,他的错误操作可能是_______。
(2)若将B装置与D装置连接可以制取的气体是_______,欲用F装置来收集废气体,则B装置的导管应与F装置的_______端(填“a”或“b”)连接。
17.按要求写出符合题意的化学方程式。
(1)有水生成的化合反应_________
(2)有水生成的复分解反应_________;
(3)有水生成的不属于四种基本反应类型的反应_________
16.下图是A、B、C三种固体物质的溶解度曲线。请回答下列问题:
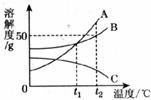
(1)在_________℃时,A、B两物质的溶解度相等;
(2)t2℃时,将相同质量的A、B、C三种固体物质分别加入到相同质量的水中,充分搅拌后都达到了饱和,则剩余固体最多的是_________;
(3)t2℃时,B物质饱和溶液的溶质质量分数为_________ (精确到0.1%)。
15.选用“>、=、<”符号填空。
(1)将盛有98%的浓硫酸的试剂瓶敞口放置于空气中,一段时间后,溶液中溶质质量分数_________98%
(2)某酸溶液的pH=A,加水稀释后的pH=B,则A_________B。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com