
28.(8分)化学与人类的生活、生产密切相关。请你利用所学的知识回答以下问题:
(1)钢铁工业的基本生产流程示意图如下:
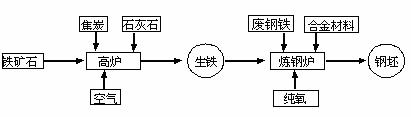
①写出以赤铁矿(主要成分为Fe2O3)为原料在高温下与一氧化碳反应制取铁的化学方程式 。
②应用化学原理分析,工业炼钢时用纯氧而不用空气的主要原因是: 。
③铁粉与生石灰都是常用的干燥剂。现欲用化学方法检验某食品袋中的干燥剂究竟是其中的哪一种?请你简述检验方法: 。
(2)氯化铁能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
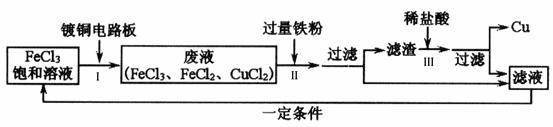
①步骤Ⅱ中发生了两个反应,其一是2FeCl3+Fe=3FeCl2,已知所含元素化合价升高的反应是氧化反应,该物质做还原剂;反之是还原反应,该物质做氧化剂。由此判断这个反应中的氧化剂是 (写化学式);
②步骤Ⅲ中发生反应的化学方程式是 ;
③该流程中可以循环、回收利用的物质是: (写化学式)。
(3)北京奥运火炬所用的燃料是丙烷(化学式为C3H8),它与甲烷(CH4)、丁烷(C4H10)、戊烷(C5H12)等属于同一系列的有机物--烷烃。根据上述几种烷烃的化学式与名称,可知:
①乙烷的化学式是_______;
②含氢量最高的烷烃的化学式是_______。
27.(4分)下面的表格中列出了氯化铵在不同温度下的溶解度:
|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度(g) |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
(1)从表中可得到的一条信息是______。
(2)20℃时,向100g水中加入50g氯化铵,形成氯化铵的_____(填“饱和”或“不饱和”)溶液;将其温度升高至60℃时,溶液的质量为_____ g,该溶液中溶质与溶剂的质量比为_______。
26.(7分)家庭厨房就是一个化学小世界,“锅碗瓢盆”和“柴米油盐酱醋茶”中包含着许多化学知识。

(1)厨房里一般有以下物品,请按材料所属类别对它们进行分类(填写字母)
A.不锈钢锅 B.大理石灶台 C.炒菜铁铲 D.PE(聚乙烯)保鲜膜
E.纯棉质的围裙 F.木质筷子
①属于金属材料的有 ;
②属于合成材料的有 。
(2)蔬菜、水果为人体所提供的主要营养素是 ,米饭、馒头等食物所含的糖类是供给人体_____的主要物质。
(3)味精(作调味品)的鲜味与溶液的酸碱度有关,当pH为6-7时鲜味最强;还与温度有关,当水溶液经120℃以上长时间加热,不仅鲜味消失,而且生成对人体有害的焦谷氨酸钠。据此,下列认识不正确的是_______(填写字母)。
A.在加热条件下生成焦谷氨酸钠是物理变化
B.菜烧熟起锅后再放味精更有利于人体健康
C.应避免在酸性或碱性较强的条件下使用味精
(4)天然气(主要成分甲烷)是很多家庭所用燃料。已知lkg甲烷燃烧生成液态水和二氧化碳,放出的热量约为5.87×104 KJ。试回答:
①参加上述反应的氧气和生成的二氧化碳的化学计量数之比(分子个数比) ;
②若lKg甲烷燃烧生成气态水和二氧化碳放出的热量 (选填“>” “<”或“=”)5.87×104kJ
25.复印机市场对纳米级四氧化三铁需求量很大,目前最普遍使用共沉淀法生产,其原理可表示为:FeCl2+FeCl3+NaOH→Fe3O4+H2O+NaCl,已知此反应中,各元素化合价均不变,又知Fe3O4中铁元素有+2、+3两种化合价。则参加反应的FeCl2和FeCl3中铁元素的质量比为
A.1∶1 B.1∶2 C.3∶4 D.2∶3
24.某气体可能由初中化学常见的一种或多种气体组成,已测定其中只含有碳、氧两种元素,且质量比为1:2,则关于该气体的说法正确的是
A.一定是纯净物 B.一定含CO
C.最多可能的组合有2种 D.可能是O2、CO2 的混合物
23.物质间存在着一定的反应关系和转化关系。下列各组物质可以按所给图示进行直接转化的是
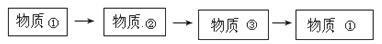
A.Fe→Fe2O3→FeSO4→Fe B.CO→CO2→H2CO3→CO
C.HCl→NaCl→CaCl2→HCl D.CO2→Na2CO3→CaCO3→CO2
22.从涂有石灰浆的墙壁上掉下一块白色固体,为了探究其成分,同学们进行如下实验:
|
实验步骤 |
实验现象 |
|
①将其研磨成粉末,加足量水搅拌 |
固体没有全部溶解 |
|
②取上层清液,滴加酚酞溶液 |
溶液呈红色 |
|
③取不溶物,滴加稀盐酸 |
有气泡产生 |
由此得出以下结论,其中正确的是
A.一定有CaCO3,可能有Ca(OH)2 B.一定有Ca(OH)2,可能有CaCO3
C.一定有CaCO3和Ca(OH)2 D.一定没有CaCO3和Ca(OH)2
21.如图所示,打开止水夹,将液体A滴入试管②中与固体B接触,若试管①中的导管口没有气泡产生,则液体A和固体B的组合可能是下列中的
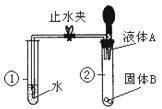
A.稀硫酸和铁 B.水和生石灰 C.盐酸和小苏打 D.水和食盐
20.比较归纳是化学学习常用的一种方法。以下是C、CH4、CO三种物质转化为CO2的转化关系,①C→CO2 ②CH4→CO2 ③CO→CO2,对它们的比较归纳正确的是
A.三种转化关系中发生的反应都属于化合反应
B.三种转化关系中所有的生成物在常温下都是气体
C.三种物质都只能跟氧气反应转化为二氧化碳
D.三种物质都能在点燃条件下转化为二氧化碳
19.对于“1+1是否一定等于2”的讨论,同学们的下列说法正确的是
A.将1 L的蒸馏水与1 L的白酒混合,所得溶液体积等于2 L
B.将1Kg的铜粉和1Kg铁粉混合,所得物质的质量等于2 Kg
C.将两杯质量分数均为1%的食盐水混合后形成溶液的质量分数是2%
D.将1 g的石灰石和1 g的盐酸反应后所形成的溶液的质量等于2 g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com