
25.第二主族元素R的单质及其相应氧化物的混合物12g,加足量水经完全反应后蒸干,得固体16g,试推测该元素可能为
A.Mg B.CA. C.Sr D.Ba
第Ⅱ卷
24.联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl.NaCl和NH4Cl共同存在时的溶解度曲线如图所示,以下操作正确的是
|
|
通入气体 |
温度控制 |
|
(A) (B) (C) (D) |
CO2 CO2 NH3 NH3 |
30~40℃ 0~10 ℃ 30~40 ℃ 0 |
22.下列离子方程式书写正确的是
A.过量氯气通入溴化亚铁溶液中 3Cl2+2Fe2++4Br-→6Cl-+2Fe3++2Br2
B.过量二氧化碳通入偏铝酸钠溶液中 CO2+2H2O+AlO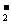 →Al(OH)3↓+HCO
→Al(OH)3↓+HCO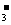
C.在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合 NH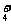 +HSO
+HSO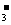 +2OH-→SO
+2OH-→SO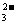 +NH3↑+2H2O
+NH3↑+2H2O
D.碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO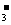 +Ca2++2OH-→CaCO3↓+2H2O+MgCO3↓
+Ca2++2OH-→CaCO3↓+2H2O+MgCO3↓
23 已知酸性强弱顺序为H2CO3> 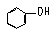 >HCO
>HCO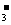 ,下列化学方程式正确的是
,下列化学方程式正确的是

21.己知维生素A的结构简式可写为 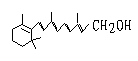
式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C.H原子未标记出来,关于它的叙述正确的是
A.维生素A的分子式为C20H30O
B.维生素A 是一种易溶于水的醇
C.维生素A分子中有异戊二烯的碳链结构
D.1mol维生素A 在催化剂作用下最多可与7molH2发生加成反应
20.某强酸溶液,强碱溶液,已知,酸碱溶液混合后,则酸溶液体积(酸)和碱溶液体积(碱)的正确关系为
A.V(酸)=102V(碱) B.V(碱)=102V(酸)
C.V(酸)=2V(碱) D.V(碱)=2V(酸)
19.根据下列反应判断有关物质还原性由强到弱的顺序是
H2SO3+I2+H2O====2HI+H2SO4
2FeCl3+2HI====2FeCl2+2HCl+I2
3FeCl2+4HNO3====2FeCl3+NO↑+2H2O+Fe(NO3)3
A.H2SO3>I->Fe2+>NO
B.I->Fe2+>H2SO3>NO
C.Fe2+>I->H2SO3>NO
D.NO>Fe2+>H2SO3>I-
18.甲.乙两烧杯中各成盛有100mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为
A.5.4g B.3.6g C.2.7g D.1.6g
17.同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3 ②NO2,进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度为
A. ①>② B. ①<② C.①=② D.不能确定
16.下列各组离子在水溶液中能大量共存的是
A.Na+ .HS- .Cu2+ .Cl- B.HS- .Na+ .OH- .K+
C.K+ .CO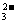 .Br- .AlO
.Br- .AlO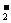 D.H+ .Cl- .Na+ .SO
D.H+ .Cl- .Na+ .SO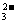
15.反应速度V和反应物浓度的关系是用实验方法测定的。化学反应H2+Cl2→2HCl的反应速度V可表示为V=K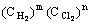 式中K为常数,m.n值可用下表中数据确定之。
式中K为常数,m.n值可用下表中数据确定之。
 (mol/L) (mol/L) |
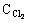 (mol/L) (mol/L) |
V(mol/L·s) |
|
1.0 |
1.0 |
1.0K |
|
2.0 |
1.0 |
2.0K |
|
2.0 |
4.0 |
4.0K |
由此可推得,m.n值正确的是
A.m=1.n=1 B.m= .n=
.n= C.m=
C.m= .n=1 D.m=1.n=
.n=1 D.m=1.n= 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com