
13.已知反应:①101Kpa时,2C(s)+O2(g)==2CO(g);△H= -221 kJ/mol
②稀溶液中,H +(aq)+OH -(aq)== H2O(1);△H= -57.3kJ/mol
下列结论正确的是
A.碳的燃烧热大于 110.5 kJ/mol
B.①的反应热为 221 kJ/mol
C.稀硫酸与稀 NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀 NaOH溶液反应生成 1mol水,放出 57.3kJ热量
第Ⅱ卷
12.我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中
的氧气与铝反应产生电流。电池总反应为:4A1+3O2+6H2O == 4A1(OH)3,
下列说法不正确的是
A.正极反应式为:O2+2H2O+4e ==40H -
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需更换铝板就可继续使用
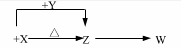
11.某温度下,体积一定的密闭容器中进行如下可逆反应:
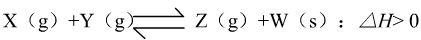
下列叙述正确的是
A.加入少量 W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.平衡后加入 X,上述反应的△H增大
10.下列关于电解质溶液的叙述正确的是
A.常温下,pH=7的 NH4Cl与氨水的混合溶液中离子浓度大小顺序为
c (CI-)>c(NH4+ ) >c ( H+ )= (OH-)
B.将 pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和 pH与体积均相同的盐酸和醋酸溶液,消耗 NaOH的物质的量相同
D.常温下,同浓度的 Na2S与 NaHS溶液相比,Na2S溶液为 pH大
9.下列说法正确的是
A.IA族元素的金属性比ⅡA族元素的金属性强
B.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D.第三周期元素的离子半径从左到右逐渐减小
8.引起下列环境污染的原因不正确的是
A.重金属、农药和难分解有饥物等会造成水体污染
B.装饰材料中的甲醛、芳香烃及氡等会造成居室污染
C.SO2、NO2 或 CO2 都会导致酸雨的形成
D.CO2 和氟氯烃等物质的大量排放会造成温室效应的加剧
7.下列说法正确的是
A.用乙醇或 CCl4可提取碘水中的碘单质
B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同
C. 24Mg 32S晶体中电子总数与中子总数之比为1:1
D.H2S和 SiF4分子中各原子最外层都满足8电子结构
27.(14分)铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是__________________________
(2)铝与氢氧化钾溶液反应的离子方程式是_________________________
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示
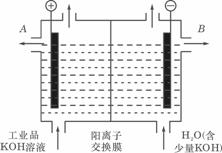
①该电解槽的阳极反应式是____________________________
②通电开始后,阴极附近溶液pH会增大,请简述原因__________________________
③除去杂质后的氢氧化钾溶液从溶液出口_________________(填写“A”或“B”)导出。 28.(14分)有X、Y、Z三种元素,已知:
①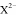 、
、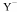 均与Y的气态氢化物分子具有相同的电子数;
均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY,ZY溶液遇苯酚呈紫色。
请回答:
(1)Y的最高价氧化物对应水化物的化学式是__________________.
(2)将ZY,溶液滴入沸水可得到红褐色液体,反应的离子方程式是___________________.
此液体具有性质是_______________(填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、燃烧后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味气体。
①已知一定条件下,每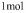 气体被
气体被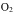 氧化放热
氧化放热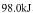 。若
。若 该气体与
该气体与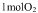 在此条件下发生反应,达到平衡时放出的热量是176.4KJ,则该气体的转化率为___________。
在此条件下发生反应,达到平衡时放出的热量是176.4KJ,则该气体的转化率为___________。
②原无色有刺激性气味的气体与含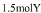 的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种氧化物,若有
的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种氧化物,若有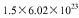 个电子转移时,该反应的化学方程式是___________________________________。
个电子转移时,该反应的化学方程式是___________________________________。
26.(17分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色瓜均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
请回答:
(1)W的电子式是____________________。
(2)X与Y在溶液中反应的离子方程是______________________。
(3)X含有四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置器中产生白色沉淀,装置V中可惧到一种无色气体。
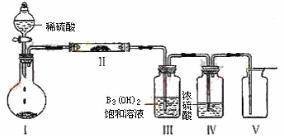
①装置I中反应的化学方程式是______________________________。
装置II中物质的化学式是_______________________________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置V中气体,该化合物的化学式是____________________,所需仪器装置是______________(从上图选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒物质,同时有X生成,该反应的化学方程式是__________________________。
25.(15分)有机物A为茉莉香型香料.

(1)A分子中含氧官能团的名称_______________________.
(2)C的分子结构可表示为(其中R和R’代表不同的烃基)
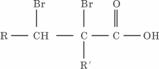
A的化学式是___________,A可以发生的反应是____________________(填写序号字母).
a.还原反应 b.消去反应 c.酯化反应 d.水解反应
(3)已知含有烃基R的有机物R-OH与浓溴水反应产生的白色沉淀,则含有烃基R’的有机物R’-OH类别属于_______________。
(4)A分子结构中只有一个甲基,A的结构简式是_____________________.
(5)在浓硫酸存在下,B与乙醇共热生成化合物C16H22O2的化学方程式是
______________________________________________________________________________.
(6)在A的多种同分异绝体中,分子结构中除烃基R’含有三个甲基外,其余部分均与A相同的有___________种.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com