
11. 在一定温度下,某无水盐R在水中溶解度为23g,向R的饱和溶液中加入 该无水盐,保持温度不变,析出R的结晶水合物Wg,从原饱和溶液中析出溶质R的质量为
该无水盐,保持温度不变,析出R的结晶水合物Wg,从原饱和溶液中析出溶质R的质量为
A.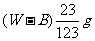 B.
B.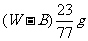
C.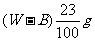 D.
D.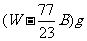
10.下列混合溶液中,各离子浓度的大小顺序正确的是
A.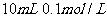 氨水与
氨水与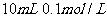 盐酸混合,
盐酸混合,
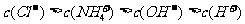
B.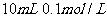
 溶液与
溶液与
 溶液混合,
溶液混合,
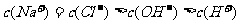
C. 溶液与
溶液与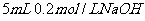 溶液混合,
溶液混合,
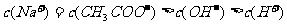
D.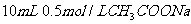 溶液与
溶液与 盐酸混合,
盐酸混合,
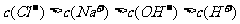
9.仅用一种试剂鉴别如下物质:苯、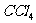 、
、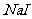 溶液、
溶液、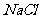 溶液、
溶液、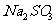 溶液,下列试剂中不能选用的是
溶液,下列试剂中不能选用的是
A.溴水 B.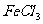 溶液
溶液
C.酸性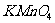 溶液 D.
溶液 D. 溶液
溶液
8.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪组原子均可产生NMR现象
A.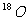
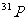
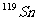
B.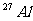
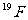
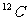
C.元素周期表中VA族所有元素的原子
D.元素周期表中第1周期所有元素的原子
7.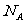 代表阿伏加德罗常数值,下列说法正确的是
代表阿伏加德罗常数值,下列说法正确的是
A.9g重水所含有的电子数为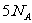
B.1molMgCl2中含有离子数为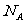
C.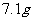 氯气与足量NaOH溶液反应转移的电子数为
氯气与足量NaOH溶液反应转移的电子数为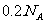
D.1molC10H20分子中共价键总数为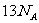
29.(12分)有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量。
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为____________________________g。
(2)乙取样品②a g强热,生成的气体不能使澄清的石灰水变浑浊。再将反应后的固体与足量的稀硝酸微热,充分反应后,有b g固体剩余,该剩余固体的化学式为_____________。样品②中氧化铜质量为_______________g (以含a、b的代数式表示)。
(3)丙称量样品③强热后剩余的固体,质量比原样品减小c g,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为________________________________________。
28.(18分)资料显示: “氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
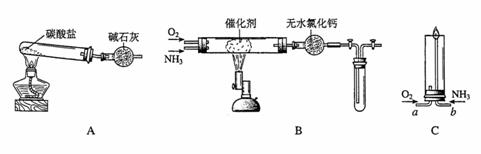
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是________________;
碱石灰的作用_____________________________________________________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是__________________________________________;
试管内气体变为红棕色,该反应的化学方程式是______________________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中试管内气体颜色变浅,请结合化学方程式说明原因_______________________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是_________________________________________________,
其理由是________________________________________________________________。
②氨气燃烧的化学方程式是__________________________________________________。
27. (15分)X、Y、Z为三个不同短周期非金属元素的单质。在一定条件下有如下反应: Y+X→A(气), Y+Z→B(气)。请针对以下两种不同情况回答:
(1)若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:
①Y的化学式是_________;
②生成固体C的化学方程式____________________________________。
(2)若常温下Y为固体,X、Z为气体, A在空气中充分燃烧可生成B,则:
①B的化学式是_______________________;
②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是
__________________________________________________________________;
③将Y与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是______________________________________________________。
26.(16分)
(1)化合物A(C4H10O)是一种有机溶剂。A可以发生以下变化:

①A分子中的官能团名称是 ;
②A只有一种一氯取代物B。写出由A转化为B的化学方程式
③A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种。
F的结构简式是 。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反
应。“HQ”还能发生的反应是(选填序号) 。
①加成反应 ②氧化反应 ③加聚反应 ④水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是 ______________.
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。
“TBHQ”与氢氧化钠溶液作用得到化学式为C10H12O2Na2的化合物。
“TBHQ”的结构简式是 。
15.下列说法正确的是
A.外界对气体做功,气体的内能一定增大
B.气体从外界吸收热量,气体的内能一定增大
C.气体的温度越低,气体分子无规则运动的平均动能越大
D.气体的温度越高,气体分子无规则运动的平均动能越大
第II卷
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com