
12.下列实验操作中,先后顺序正确的是
A 稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水
B 为测定硫酸铜晶体的结晶水含量,称样时,先称取一定量的晶体,后放入坩埚
C 为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后硝酸钡溶液
D 在制取干燥纯净的氯气时,先使氯气通过水(或饱和食盐水),后通过浓硫酸
11.下列有关pH变化的判断中,正确的是
A 随着温度的升高,碳酸钠溶液的pH减小
B 随着温度的升高,纯水的pH增大
C 新氯水制经光照一段时间后,pH减小
D 氢氧化钠溶液久置于空气中,pH增大
10.将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是
A Mg、AlCl3、NaAlO2 B KNO3、NaCl、CH3COONa
C NaClO、Na2SO3、BaCl2 D Ba(NO3)2、FeSO4、NH4HCO3
9.下列说法正确的是
A 含有相同氧原子数的SO2和CO的质量相等
B 等物质的量浓度的NaOH溶液与氨水中的c(OH-) 相等
C 乙酸分子与甲酸甲酯分子中的共价健数相等
D 等温等压下,3mol C2H2(g)和1mol C6H6(g)的密度相等
8.右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
A 常压下五种元素的单质中Z单质的沸点最高
B Y、Z的阴离子电子层结构都与R原子的相同
C W的氢化物沸点比X的氢化物的沸点高
D Y元素的非金属性比W元素的非金属性强
7.在一定温度不同压强(p1<p2)下,可逆反应2X(g)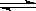 2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(
2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(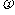 )与反应时间(t)的关系有以下图示,正确的是
)与反应时间(t)的关系有以下图示,正确的是

A B C D
6.高压电机、复印机工作时会产生臭氧,该气体有强氧化性。下列叙述中不正确的是
A 臭氧和氧气是氧的同素异形体 B 臭氧可使湿润的KI淀粉试纸变蓝
C 臭氧的存在对人体有益无害 D 臭氧是很好的消毒剂和脱色剂
29.(15分)苏丹红一号(sudan Ⅰ)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2-萘酚为主要原料制备的,它们的结构简式如下所示:

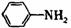
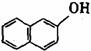
(苏丹红一号) (苯胺) (2-萘酚)
(提示: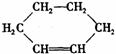 可表示为
可表示为 )
)
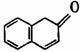
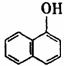
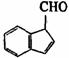
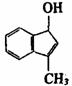
(A) (B) (C) (D)
(1)苏丹红一号的化学式(分子式)为
(2)在下面化合物(A)-(D)中,与2-萘酚互为同分异构体的有(填字母代号) 。
(3)上述化合物(C)含有的官能团是
(4)在适当的条件下,2-萘酚经反应可得到芳香化合物E(C8H6O4),1molE与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),E与溴在有催化剂存在时反应只能生成两种一溴代物,两种一溴代物的结构简式分别是 ,E与碳酸氢钠反应的化学方程式是 。
(5)若将E与足量乙醇在浓硫酸作用下加热,可以生成一个化学式(分子式)为C12H14O4的新化合物,该反应的化学方程式是 ,反应类型是 。
28.(15分)已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
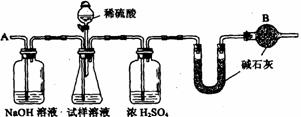
主要实验步骤如下:①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果 (填高、偏低或不变)
(4)步骤⑤的目的是
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验法。
27.(15分)甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是 。
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途: 。
(3)在一定条件下,甲与O2反应的化学方程式是 。
(4)丁的元素符号是 ,他的原子结构示意图为 。
(5)丁的氧化物的晶体结构与 的晶体结构相似。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com