
8.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3+N2+3C 2AlN+3CO,下列叙述正确的是
2AlN+3CO,下列叙述正确的是
A. 在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B. 上述反应中每生成2 mol AlN,N2得到3 mol电子
C. 氮化铝中氮元素的化合价为-3价
D. 氮化铝晶体属于分子晶体
7.下列离子反应方程式书写正确的是
A.在Ba(OH)2溶液中加入少量的硫酸氢钠溶液Ba2++2OH-+2H++SO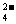 =BaSO4↓+2H2O
=BaSO4↓+2H2O
B.向次氯酸钙溶液中通入SO2气体Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.标准状况下,将112mLCl2缓慢注入10mL 1mol·L-1的FeBr2溶液中
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
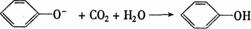 D.向苯酚钠溶液中通入少量CO2气体
D.向苯酚钠溶液中通入少量CO2气体
+HCO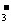
6. 下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是
A.氯化镁、氢氧化钠 B.硫酸钠、氢氧化钡
C.氯化铝、氨水 D.溴化亚铁、氯水
5.下列反应中生成物总能量高于反应物总能量的是
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
4.下列事实与氢键有关的是
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.C H4 SiH4 SnH4熔点随相对分子质量增大而升高
D.HF HCl HBr HI 的热稳定性依次减弱
3. 右图是同学们经常使用的某品牌修正液包装标签。小明仔细阅后,结合自己的生活经验和所学知识得出了该修正液的某些性质,小明的推测中不合理的是
右图是同学们经常使用的某品牌修正液包装标签。小明仔细阅后,结合自己的生活经验和所学知识得出了该修正液的某些性质,小明的推测中不合理的是
A.修正液是一种胶体,均一、透明
B.修正液中含有的化学物质有毒
C.修正液的成分对纸张不具有腐蚀性
D.修正液的溶剂易挥发、易燃
2.下列分子中,所有原子都满足最外层为8电子结构的是
A.CO2 B.SiH4 C.SF6 D.PCl5
1.下列叙述中,错误的是
A.离子化合物中可能存在共价键 B.原子晶体中一定存在共价键
C.分子晶体中一定存在共价键 D.含有离子键的化合物形成的晶体一定是离子晶体
30. Fe和Al是两种常用的金属,将它们按一定的质量比组成混合物。
(1)取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,则反应的离子方程式为 ,混合物中的Al的物质的量为 。(用含字母的数学式表示)
(2)另取相同质量的该混合物,向其中加入足量的稀硫酸,固体全部溶解,生成气体的体积在标准状况下为m L,则反应中转移电子的物质的量为 ,混合物中Fe的质量为 。(用含字母的数学式表示)
(3)向(2)所得的溶液中加入过量的氢氧化钠溶液,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体, 经称量发现该固体的质量和原混合物的质量恰好相等,则原混合物中铝的质量分数为 。
29. 已知A、B、C、D分别代表中学化学常见物质(或微粒),其中A、B均为两种元素组成的化合物(或微粒),相互转化关系见下图(有关反应条件已略去).
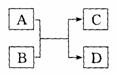
请根据题目要求回答下列问题:
(1)若A、B两化合物相互反应得到气体单质C和化合物D,则化学方程式为(只写一个):________________________________________________________________;
(2)若A、B两化合物相互反应生成非金属固体单质C和化合物D,且A的相对分子质量大于B,则A、B的化学式为:A________________、B________________,该反应中氧化产物与还原产物的物质的量之比为________________;
(3)若A为5个原子构成的微粒,且A、B均为10电子微粒,含适量A、B微粒的溶液在加热条件下反应生成气体C和化合物D,则A微粒的电子式为________________,C分子的空间构型为________________,含A、B微粒的溶液转化为C、D的离子方程式为___________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com