
18.已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。
下列判断正确的是
A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2 B.上述实验中,共有两个氧化还原反应 C.实验①生成的气体有可能使湿润的淀粉KI试纸最终仍呈白色 D.实验②证明Fe2+既有氧化性又有还原性
17.下列各选项所述的两个量,前者一定大于后者的是
① HBr和HF的沸点 ②纯水在25℃和80℃时的pH值
③ SiC和金刚石的熔点
④ 25℃时,等体积的pH值都等于3的盐酸和AlCl3溶液中,由水电离产生的H+浓度
⑤ 在NH3+NO→N2+H2O(未配平)反应中,被氧化和被还原的N原子数
⑥ 耐火材料MgO和CaO的熔点 ⑦ H-和H+离子半径
A . ①②⑥⑦ B. ①②③⑤ C . ②⑥⑦ D . ⑤⑥⑦
16.还原2.4×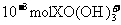 到X元素的低价态时,需消耗30mL0.2mol·
到X元素的低价态时,需消耗30mL0.2mol·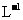 的亚硫酸钠溶液,则在此反应中X元素的低价态为
的亚硫酸钠溶液,则在此反应中X元素的低价态为
A.0价 B.+1价 C.-1价 D.-2价
15.可以将反应Zn+Br2=ZnBr2设计成蓄电池,下列4个电极反应
①Br2+2e-=2Br- ②2Br--2e-=Br2 ③Zn-2e-=Zn2+ ④Zn2++2e-=Zn
其中表示正极反应和负极反应的分别是
A.①和③ B.②和① C.③和① D.④和①
14.在酸性溶液中存在着大量的NH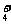 、K+和Ba2+三种阳离子,还可能存在
、K+和Ba2+三种阳离子,还可能存在
①HCO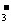 、②NO
、②NO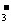 、③SO
、③SO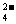 、④CO
、④CO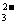 、⑤AlO
、⑤AlO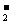 五种阴离子中的
五种阴离子中的
A. 只有① B.只有② C. ③和⑤ D. ②和③
13.在硫酸、明矾和硫酸钾组成的混合溶液中,c(Al3+)=0.4 mol·L-1,c(SO42-)=0.8mol·L-1, 水电离的[H+]=10-13 mol·L-1,则c(K+)为
A. 0.15 mol·L-1 B.0.2 mol·L-1
C. 0.3 mol·L-1 D.0.4 mol·L-1
12.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的是离子组是
A. K+、Na+、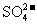 、
、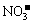 B. Na+、
B. Na+、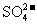 、Cl-、ClO-
、Cl-、ClO-
C. H+、Mg2+、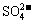 、
、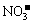 D. Ag+、K+、
D. Ag+、K+、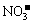 、Na+
、Na+
11.已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1); △H=-4b kJ/mol
B.C2H2(g)+2.5O2(g)=2CO2(g)+H2O(1); △H=2b kJ/mol
C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1); △H=-2b kJ/mol
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1); △H=b kJ/mol
10. 下列关于晶体的说法一定正确的是
下列关于晶体的说法一定正确的是
A.分子晶体中都存在共价键
B. CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C. SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
9.已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2氧化性依次减弱。下列反应在水溶液中不可能发生的是
A.3 Cl2 + 6 FeI2 = 2FeCl3 + 4 FeI3 B.Cl2 + FeI2 = FeCl2 + I2
C.Co2O3 + 6 HCl = 2CoCl2 + Cl2↑+ 3H2O D.2Fe3+ + 2I- = 2Fe2+ + I2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com