
6.在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)=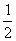 N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g);ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度
B.加催化剂同时增大压强
C.升高温度同时充入N2
D.降低温度同时增大压强
5.现有三组混合液:①乙酸乙酯和乙酸钠溶液 ②乙醇和丁醇 ③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D. 蒸馏、萃取、分液
4.下列叙述从化学角度分析,其中错误的是
A.被蜜蜂蛰咬后,可涂抹稀氨水或小苏打溶液减轻疼痛
B.HgCl2的稀溶液可用于手术器械消毒,原因是可使蛋白质凝固
C.燃料煤脱硫后使用,可减少对大气的污染
D.氟利昂(CCl2F2)或NOx都可破坏臭氧层,而导致“温室效应”
3.下列说法错误的是
A.原子晶体中只存在非极性共价键
B.分子晶体的状态变化,只需克服分子间作用力
C.金属晶体通常具有导电、导热和良好的延展性
D.离子晶体在熔化状态下能导电
2.2002年瑞典科学家发现,某些高温油炸食品中含有一定量的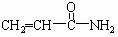 (丙烯酰胺)。食品中过量的丙烯酰胺可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述:
(丙烯酰胺)。食品中过量的丙烯酰胺可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述:
①能使酸性KMnO4溶液褪色 ②能发生加聚反应生成高分子化合物
③只有4种同分异构体 ④能与氢气发生加成反应
其中正确的是
A.①②③ B.②③④ C.①③④ D.①②④
1.保护环境是每一个公民的责任。下列做法:( )
①推广使用无磷洗涤剂 ②城市生活垃圾分类处理
③推广使用一次性木质筷子 ④推广使用清洁能源
⑤过量使用化肥、农药 ⑥推广使用无氟冰箱。
其中有利于保护环境的是
A.①②④⑤ B.②③④⑥ C.①②④⑥ D.③④⑤⑥
29.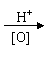 (16分)已知:
(16分)已知:
(1)CH3CH=CH2 HCOOH + CH3COOH
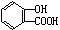
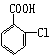
(2)水杨酸的结构简式为
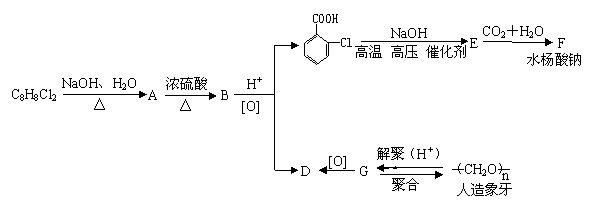 对下列物质有如图所示的转化关系:
对下列物质有如图所示的转化关系:
试根据上述信息结合所学知识回答:
(1)A的结构简式 ;
 (2)写出D物质中所含官能团的名称
;
(2)写出D物质中所含官能团的名称
;
(3) 生成E的反应中所消耗NaOH的物质的量是 ,其反应类型为
;
(4)写出人造象牙解聚成G的化学方程式 ;
(5)写出E生成F的离子方程式 ;
28.(13分)在Mg(NO3)2和Al(NO3)3的混合溶液中,NO3-的物质的量为0.7mol。向该溶液中加入100mL 8mol·L-1的KOH溶液,使之充分反应。反应前,若Al3+的物质的量与混合溶液中离子总物质的量的比值为x。(不考虑Mg2+和Al3+的水解及水的电离所引起的离子总数的变化)
(1)x的取值范围是____________________________________。
(2)当KOH刚好完全消耗,且Al3+全部转化为AlO2-时,x的值为___________________。
(3)将(2)中的x的值记为x1,则当0<x≤x1时,反应生成的沉淀物的化学式为_____________,当x> x1时反应生成的沉淀物的化学式为_____________ 。
(4)若反应前Al3+的物质的量为a mol,则a=_____________(用含x的代数式表示) 。
27.(14分)某厂废液中含有大量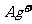 、
、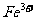 、
、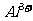 ,用下列图示方法进行分离(部分反应条件省略):
,用下列图示方法进行分离(部分反应条件省略):
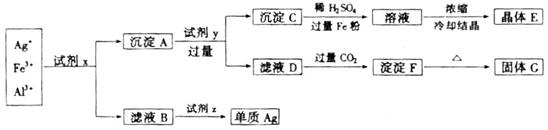
(1)写出下列物质的化学式:
试剂x_______________、试剂z_______________。
晶体E_______________、固体G_______________
(2)写出下列反应的离子方程式:
沉淀A+试剂y:_______________ 滤液D+过量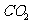 :_____________________
:_____________________
26.(本题15分)
I. 近期,科学家用NaNO3和Na2O在573K反应制得了离子化合物Na3NO4。
(1)经测定,Na3NO4中各原子最外层电子数都达到了8电子稳定结构,则NO43-的电子式为______________________。
(2) Na3NO4与CO2或H2O都能剧烈反应,并转化为常见物质,写出这两个反应的化学方程式:________________________________、_________________________________。
II. 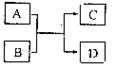 已知A、B、C、D分别代表中学化学常见物质(或粒子),其中A、B均为两种元素组成的化合物(或粒子),相互转化关系如右图(有关反应条件已略去)。请根据题目要求回答下列问题:
已知A、B、C、D分别代表中学化学常见物质(或粒子),其中A、B均为两种元素组成的化合物(或粒子),相互转化关系如右图(有关反应条件已略去)。请根据题目要求回答下列问题:
(1)若A、B两化合物相互反应生成非金属固体单质C和化合物D,且A的相对分子质量大于B的相对分子质量,则A、B的化学式分别为A________、B________,该反应中,氧化产物与还原产物的物质的量之比为____________。
(2)若A为5个原子构成的粒子,且A、B均为10电子粒子,含适量A、B粒子的溶液在加热条件下反应生成气体C和化合物D,则A的化学式为__________,C分子的空间构型为____________,含A、B粒子的溶液转化为C、D的离子方程式为_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com