
12.下列实验操作或事故处理中,正确的做法是
A.银镜反应实验后附有银的试管,可用稀H2SO4清洗
B.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次
C.不慎将浓硫酸沾在皮肤上,立即用NaOH溶液冲洗
D.在250mL 烧杯中,加入216mL水和24gNaOH固体,配制10%NaOH溶液
11.在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
A.两种气体的压强相等 B.O2比O3的质量小
C.两种气体的分子数目相等 D.两种气体的氧原子数目相等
10.下列离子方程式正确的是
A.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
B.澄清石灰水与少量小苏打溶液混合:Ca2+ + OH- + HCO3‑ →CaCO3↓ + H2O
C.等体积等物质的量浓度的NaOH和NH4HSO4溶液混合:H+ + OH- = H2O
D.醋酸洗涤铜器表面的碱式碳酸铜: Cu2(OH)2CO3 +4H+ = 2Cu2+ +CO2↑+3H2O
9.ClO2是一种消毒杀菌效率高的水处理剂,实验室可通过以下反应制得:KClO3+H2C2O4+H2SO4→ClO2+K2SO4+CO2↑+H2O(末配平)。下列有关的叙述中,正确的是
A.ClO2是氧化产物
B.还原产物与氧化产物的物质的量之比为1:2
C.H2C2O4的还原性比ClO2强
D.1 mol KClO3参加反应时有1 mol电子发生转移
8.向100 mL FeBr2溶液中通入标准状况下的Cl2 3.36 L,Cl2 全部被还原,测得溶液中c(Br-)=c(Cl-),则原FeBr2溶液的物质的量浓度为
A.0.75 mol·L-1 B.2 mol·L-1 C.1.5 mol·L-1 D.3 mol·L-1
7.已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
6.25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2 800 kJ/mol,则下列热化学方程式正确的是
A.C(s)+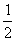 O2(g)=CO(g);△H=-393.5 kJ/mol
O2(g)=CO(g);△H=-393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(g);△H=+571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3 kJ/mol
D.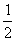 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1 400 kJ/mol
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1 400 kJ/mol
5.下列说法正确的是
A.200 mL,1 mol/L Al2(SO4)3溶液中,Al3+ 和SO42-离子总数为6.02×1023
B.标准状况下,22.4 L Cl2和HCl的混合气体中含分子总数为2×6.02×1023
C.30 g甲醛中含共用电子对总数为4×6.02×1023
D.0.1 mol 8135Br原子中含中子数为3.5×6.02×1023
4.钠盐和钾盐性质相似,但在实际生产中多用钾盐而不用钠盐。如在实验室制氧气是用 KClO3而不是用NaClO3,制黑火药用KNO3而不用 NaNO3,并且在KNO3中不能含有NaNO3,对此现象,以下各种理由合理的是
A.钠盐比钾盐更容易得到 B.钾盐的氧化性比钠盐弱
C.钠盐的吸湿性比钾盐强 D.钾盐的熔点比钠盐高
3.关于化工生产的下列叙述中,不正确的是
A.工业生产硫酸时,使用热交换器可以充分利用反应热
B.工业上合成氨没有采用更大的压强是从设备和动力要求方面考虑的
C.工业上用离子交换膜法电解饱和食盐水生产烧碱
D.工业上采用电解熔融氯化铝生产金属铝
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com