
37.(4分)某温度下22%NaNO3溶液150毫升,加100克水稀释后浓渡变成14%.求原溶液的摩尔浓度.
36.(3分)羧酸酯RCOOR′在催化剂存在时可跟醇R″OH发生如下反应 (R′,R″是两种不同的烃基):

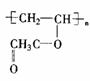
此反应称为酯交换反应,常用于有机合成中.
在合成维纶的过程中,有一个步骤是把聚乙酸乙烯酯转化成聚乙烯醇,这一步就是用过量的甲醇进行酯交换反应来实现的.
(1)反应中甲醇为什么要过量? .
(2)写出聚乙烯醇的结构简式: .
(3)写出聚乙酸乙烯酯与甲醇进行酯交换反应的化学方程式:
.
35.(5分)A是一种酯,分子式是C14H12O2.A可以由醇D跟羧酸C发生酯化反应得到.A不能使溴(CCl4溶液)褪色.氧化B可得到C.
(1)写出A、B、C结构简式:
A B C
(2)写出B的两种同分异构体的结构简式,它们都可以跟NaOH反应.
和 .
34.(4分)卤代烃在氢氧化钠存在的条件下水解,这是一个典型的取代反应.其实质是带负电的原子团(例如OH-等阴离子)取代了卤代烃中的卤原子.例如:
CH3CH2CH2-Br+OH-(或NaOH)→CH3CH2CH2-OH+Br-(或NaBr)
写出下列反应的化学方程式:
(1)溴乙烷跟NaHS反应: .
(2)碘甲烷跟CH3COONa反应: .
(3)由碘甲烷、无水乙醇和金属钠合成甲乙醚(CH3-O-CH2CH3): .
33.(4分)某待测液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、NH 4+
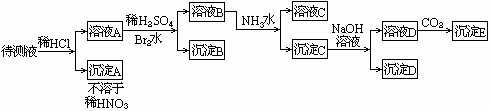
等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的)。
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由.答: .
(2)写出沉淀D的分子式: .
(3)写出从溶液D生成沉淀E的反应的离子方程式: .
32.(2分)在金刚石的网状结构中,含有由共价键形成的碳原子环,其中最小的环上有 (填数字)个碳原子,每个碳原子上的任意两个C-C键的夹角都是 (填角度).
31.(2分)气态氯化铝(Al2Cl6)是具有配位键的化合物,分子中原子间成键的关系如下图所示.请将图中,你认为是配位键的斜线上加上箭头.
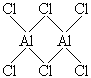
30.(2分)配平下列化学方程式:

29.(9分)将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现.这是因为通气后混和液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出.
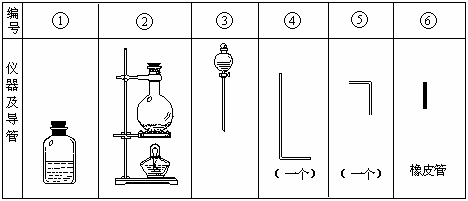
进行此实验,所用的仪器及导管如图.
根据要求填写下列空白:
(1)组装氯气发生器时,应选用的仪器及导管(填写图中编号)是 .
(2)实验进行中,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次是 .
(3)仪器①的橡皮塞上应有 个孔,原因是 .
(4)实验时,仪器①中除观察到红光外还有 现象.
(5)实验需用约10%H2O2溶液100毫升,现用市售30%(密度近似为1克/厘米3)H2O2来配制,其具体配制方法是 .
(6)实验时仪器①中ClO-与H2O2反应的离子方程式是 .
28.(2分)Cu+在酸性溶液中不稳定,可发生自身氧化-还原反应生成Cu2+和Cu.现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸,而没有其它试剂.简述如何用最简便的实验方法来检验CuO经氢气还原所得到的红色产物中是否含有碱性氧化物Cu2O.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com