
26、 (12分)孔雀石和石青是自然界存在的两种碳酸盐类铜矿,它们的化学组成可表示为:
xCuCO3•yCu(OH)2 (x、y为正整数且x≤2,y≤2)
(1)孔雀石和石青分别与过量盐酸反应时,孔雀石耗用的盐酸的物质的量与生成的CO2的物质的量之比为4:1;石青则为3:1。请推算它们的化学组成。
孔雀石: 石青:
(2)现有孔雀石和石青混合样品,取两份等质量的样品,在一份中加入过量盐酸,生成CO2 3.36L(标准状况下);加热另一份样品使其完全分解,得到CuO 20g,试通过计算确定该混合物中孔雀石和石青的物质的量之比。
25、 (8分)维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知浓度的I2溶液进行滴定。该反应的化学方程式如下:
C6H8O6 + I2 = C6H6O6 + 2HI
现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下。取10mL 6mol/LCH3COOH,加入100mL蒸馏水,将溶液加热煮沸后放置冷却。精确称取0.2000g样品,溶解于上述冷却的溶液中。加入1mL淀粉指示剂,立即用浓度为0.05000mol/L的I2溶液进行滴定,直至溶液中的蓝色持续不褪为止,共消耗21.00mL I2溶液。
(1) 为何加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用?
(2) 计算样品中维生素C的质量分数。
24、 (10分)
(1)具有支链的化合物A的分子式为C4H9O2,A可以使Br2的四氯化碳溶液褪色。1molA
和1mol NaHCO3能完全反应,则A的结构简式是 。写出与A具有相同官能团的A的所有同分异构体的结构简式
。
(2)化合物B含有C、H、O三种元素,分子量为60,其中碳的质量分数为60%,氢的质量分数为13.3%。B在催化剂Cu的作用下被氧气氧化成C,C能发生银镜反应,
则B的结构简式是
(3)D在NaOH水溶液中加热反应,可生成A的钠盐和B,相应反应的化学方程式是
23、 (8分)根据下面的反应路线及所给信息填空。
ACl2,光照①
 NaOH,乙醇△,②
NaOH,乙醇△,②
 Br2的CCl4溶液③
Br2的CCl4溶液③ B④
B④

(一氯环已烷)
(1)A的结构简式是 ,名称是 。
(2)①的反应类型是 ,③的反应类型是 。
(3)反应④的化学方程式是
22、 (10分)我国研制的长征捆绑式火箭在第一、二级发动中用“编二甲(基)肼”和四氧化二氮作为液体燃料。
(1) 已知偏二甲(基)肼的相对分子质量为60,其中含碳40%,含氢13.33%,其余为氮;又知其分子中有一个氮原子不与氢原子相连。通过计算写出偏二(基)肼的化学式和分子结构简式:
(2)在发动机中偏二甲(基)肼在四氧化二氮中充分燃烧,写出该燃烧反应的化学方程式(反应中所有的氮元素均转化为N2)。
21、 (10分)A、B、C、D是四种可溶的化合物,分别由阳离子K+、Ba2+、Al3+、Fe3+和阴离子OHˉ、CO32ˉ、NO3ˉ、SO42ˉ两两组合而成,它们的溶液发生如下反应:
A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失。
C与D反应生成有色沉淀。
B与C反应生成白色沉淀。
写出它们的化学式:
A: B: C: D:
20、 (16分)海水的综合利用可以制备金属镁,其流和如下图所示:

(1) 若在空气中加热MgCl2•6H2O,生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式
用电解法制取金属镁时,需要无水氧化镁。在干燥的HCl气流中加热MgCl2•6H2O时,能得到无水MgCl2,其原因是
(2) Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。
(3) 实验室时将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:
过滤时:
蒸发时:
19、用仪器A、B和胶管组成装置收集NO气体,(①仪器A已经气密性检查;②除水外不能选择其他试剂。)
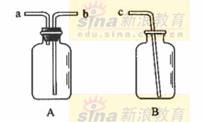
正确的操作步骤是_________________________________________________________。
18、 右图曲线a表示放热反应 X(g) + Y(g) 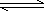 Z(g) + M(g) + N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g) + M(g) + N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
A、升高温度 B、加大X的投入量
C、加催化剂 D、增大体积
第Ⅱ卷
17、 已知葡萄糖的燃烧热是2804kJ/mol,当它氧化生成1g水时放出的热量是
A、26.0kJ B、51.9kJ C、155.8kJ D、467.3kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com