
23、氢叠氮酸(HN3与醋酸酸性相近,基其盐稳定,但撞击发生爆炸生成氮气,有关氢叠氮酸的叙述有①NaN3的水溶液呈碱性;②HN3的固体属于分子晶体;③NaN3的固体属于离子晶体; ④NaN3可用于小汽车防撞保护气囊。其中正确的是
A、①②③ B、②③④ C、①③④ D、全部
24 按下列实验方法制备气体,合理又实用的是
A、锌粒与稀硝酸反应制备氢气
B、向饱和氯化钠溶液中滴加浓硫酸制备HCl
C、亚硫酸钠与浓硫酸反应制备SO2
D、大理石与浓硫酸反应制备CO2
22、下列说法中正确的是
A、1mol稀硫酸和1mol稀Ba(OH)2溶液完全中和所放出的热量为中和热。
B、中和反应都是放热反应,盐类水解反应都是吸热反应。
C、在101kPa时,1mol碳燃烧所放出的热量一定是碳的燃烧热。
D、碳与二氧化碳的反应既是吸热反应,也是化合反应。
21.下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是
A、NaHSO4和Ba(OH)2 B、AlCl3和NaOH
C、NaAlO2和H2SO4 D、Ba(HCO3)2和Ba(OH)2
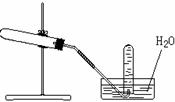
20、下图装置可用于
(A)加热无水醋酸钠和碱石灰混合物,制取甲烷
(B)加热硝酸铅制取二氧化氮
(C)加热氯酸钾和少量二氧化锰,制取氧气
(D)加热氯化铵和消石灰混合物,制取氨气
19.近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为KI+3H2O=KIO3+3H2↑。下列有关说法中正确的是
A、电解时,石墨作阳极,铁作阴极
B、电解时,在阳极上产生氢气
C、电解过程中,每转移0.6mol电子,理论上可得到0.1mol无水KIO3晶体
D、电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧
18.下列反应的离子方程式错误的是
A、向碳酸氢钙溶液中加入过量氢氧化钠
Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
B、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢氨溶液混合
Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3·H2O+H2O
C、过量CO2通入氢氧化钠溶液中 CO2+2OH-=CO32-+H2O
D、氢氧化铝与足量盐酸反应 Al(OH)3+3H+=Al3++3H2O
17.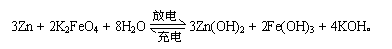 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。
高铁电池的总反应为:
下列叙述不正确的是
A.放电时负极反应为:Zn-2e- +2OH- = Zn(OH)2
B.充电时阳极反应为:Fe(OH)3 -3e- + 5OH- = FeO42- + 4H2O
C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
16.下列描述中,不符合生产实际的是
A.电解熔融的氧化铝制取金属铝,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在镀件上电镀锌,用锌作阳极
15.某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3∶1。用石墨作电极电解该混合溶液时,根据电极产物,可明显分为三个阶段。下列叙述不正确的是
A.阴极自始自终只析出H2 B.溶液pH不断增大,最后为7
C.电解最后阶段为电解水 D.阳极先析出C12,后析出O2
14.下列实验中用错试剂的是:
A、用稀盐酸清洗做焰色反应的镍铬丝; B、用酒精萃取碘水中的碘;
C、用稀硝酸洗去残留在试管壁上的铜; D、用碱石灰吸收氨气中的水蒸气
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com