
5.有机物硫醇RSH与醇ROH相似。若乙酸与CH3SH在一定条件下发生酯化反应,则所生成的酯为
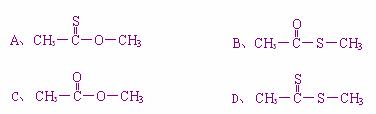
4.设NA为阿伏加德罗常数,下列叙述中正确的是( )
A.标准状况下22.4L PCl3中含有的原子数为4NA
B.标准状况下22.4L NO2中含有的原子数为3NA
C.1mol FeCl3若完全水解可以形成NA个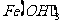 胶粒
胶粒
D.2.90g 熟石膏(2CaSO4·H2O)晶体中结晶水的数目0.01NA个
3.以下化学用语正确的是
A.乙炔的结构简式CHCH B.乙酸的最简式CH2O
C.氨气的结构式为 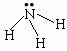 D.氯化钠的电子式
D.氯化钠的电子式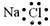
2.在一定条件下的密闭容器中投入4 molA和n molB,发生如下反应4A+5B
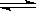 4C+6D。达到平衡时,测得A的转化率大于B的转化率。则n的取值范围正确的是( )
4C+6D。达到平衡时,测得A的转化率大于B的转化率。则n的取值范围正确的是( )
A.n=5 B.n<5 C.n>5 D.n=4
1.下列混合物不可能属于胶体的是( )
A.固体+气体 B.液体+气体 C.气体+气体 D.固体+固体
22.(12分)
铜元素的化合物往往呈现出五颜六色,如铜器久置于空气中会跟水蒸气、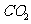 、
、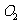 反应产生“铜锈”,即碱式碳酸铜(
反应产生“铜锈”,即碱式碳酸铜(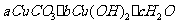 )是绿色固体。
)是绿色固体。
(1)用连线的方法说明下列含铜化物的颜色。
例:[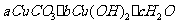 ]----绿色
]----绿色
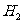
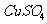 黑色
黑色
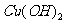 红色
红色
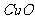 蓝色
蓝色
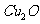 白色
白色
(2)现设计一个实验,确定[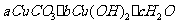 ]种a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
]种a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解 ③________________④____________⑤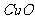 称量
称量
(3)已知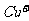 在酸性溶液种布稳定,可发生自身氧化还原方应生成
在酸性溶液种布稳定,可发生自身氧化还原方应生成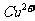 和
和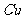 。实验室用适量
。实验室用适量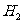 还原8.00g
还原8.00g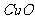 ,得到红色固体A,向A中加入足量稀硫酸,充分反应后得5.76g红色固体B。
,得到红色固体A,向A中加入足量稀硫酸,充分反应后得5.76g红色固体B。
红色固体A的成份是__________,红色固体A 中各成份的质量分别是___________。
21.(12分)
小表中的实线表示元素周期表的部分边界。①-⑤分别表示元素周期表中对应位置的元素。
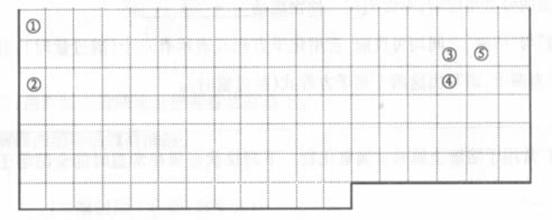
(1)请再上表中用实线补全元素周期表边界。
(2)元素③④⑤氢化物的稳定性由强到弱的顺序是_____________(用氢化物的化学式表示)
(3)元素③一般再化合物中显________价,但在与_______形成化合物时,所显示的价态正好相反。
(4)A、B两种化合物均由①②③④四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式____________________。
(5)X、Y、Z代表原子序数一次增大的三种短周期元素。在周期表中,Y与X相邻,Y与Z也相邻;X、Y和Z三种元素原子的最外层电子数之和为17
X、Y、Z三种元素有的是上表中编号①-⑤的元素,有的不是,请在上表中用元素符号标出不是①-⑤元素的相应位置。
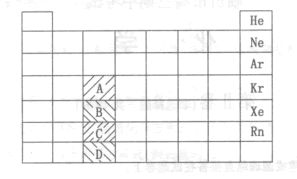
(6)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则可以排布118种元素。
某同学受镧系、锕系元素排列方式的启发,将元素周期表设计成下列更简明的形式,把118种元素全部排列在内,表中除A、B、C、D外每个位置只表示一种元素。
则该表中的A位置包含_______(填数字)种元素。C位置种的元素是否全部是金属元素___________(选填“是”或“否”)。
20.(7分)
A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,甲、乙、丙为常见化合物。他们之间有如下转化关系。
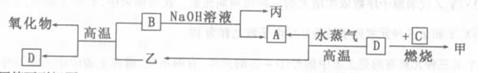
回答下列问题:
(1)B与
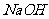 溶液反应的离子方程式是_________________;
溶液反应的离子方程式是_________________;
D与甲溶液反应的离子方程式是____________________。
(2)一定条件下,2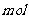 B与3
B与3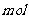 D的氧化物W恰好完全反应生成D和另一种氧化物,则W是_____________。
D的氧化物W恰好完全反应生成D和另一种氧化物,则W是_____________。
(3)将甲的浓溶液滴入到沸水中,并继续加热能得到红褐色的液体,区别该分散系是胶体还是溶液的最简便方法称为__________________。
19.(9分)
化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的酚类角度看,不恰当的一种物质是______.
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时)。_________________
(3)“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是__________。
A.Ag B.Cu C.Al D.Fe
(4)烧碱。纯碱均可吸收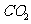 ,当含0.1mol
,当含0.1mol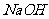 的溶液吸收一定量
的溶液吸收一定量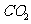 后,将溶液低温蒸干得到固体的组成可能有四种情况,分别是:
后,将溶液低温蒸干得到固体的组成可能有四种情况,分别是:
①______________ ②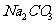 ③______________ ④
③______________ ④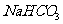
将得到的固体重新溶解于水,在溶液中加盐酸,使溶液的PH=7,再将溶液蒸干,得到固体的质量是______g。
18.(9分)
食盐是人类生活不可缺少的物质,海水中含有大量食盐。
(1)炒菜时,不慎将盐粒撒落再灶火上,会使本来蓝色的火焰呈现黄色,该现象称为_____反应。
(2)某地出产的粗盐中,所含杂质是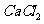 ,通过下面的实验可确定该粗盐样品中
,通过下面的实验可确定该粗盐样品中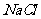 的纯度,并制得纯净的
的纯度,并制得纯净的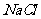 。
。
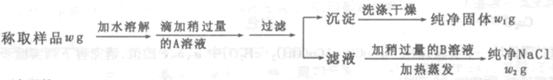
请回答:
①加入的A是_______,检验A已过量的方法是_________________________________.
②加入的B是_____________。加入稍过量B的目的是____________________________。
③为检验沉淀是否洗净,最好再最后几滴洗出液中加入______________溶液。
④该样品中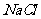 的质量分数的计算式是___________________
的质量分数的计算式是___________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com