
5.下列实验操作正确的是
A.粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体
B.容量瓶检漏:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,反复倒置数次,观察是否漏水
C.不慎将浓苛性钠溶液沾到皮肤上,立即用H2SO4 中和并洗涤
D.测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较
4.ClO2 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:
 ;下列说法正确的是
;下列说法正确的是
A.KClO3在反应中得到电子
B.ClO2 是氧化产物
C.H2C2O4在反应中被还原
D.1 mol KClO3 参加反应有 2 mol 电子转移
3.下列叙述正确的是
A.变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
B.禽流感并不可怕,当加热到70℃以上就可以使其病毒蛋白质凝聚变性而致死,日常使用的消毒剂也可以用于杀灭该病毒
C.棉花、羊毛、木材和草类的主要成分都是纤维素
D.误食重金属盐引起人体中毒,此时可喝大量的食盐水解毒
2.下列说法正确的是
A.海轮船壳上镶嵌锌块能起到防止钢铁腐蚀的作用,如果漆层脱落,则锌起不到保护作用
B.乙醇是可再生能源,而且比汽油污染小,应大力推广“乙醇汽油”
C.光导纤维非常细导光能力非常强,能同时传输大量信息,光导纤维是由硅晶体制成的
D.工业制硫酸尾气中,常含SO2 等有害气体,如果直接排入大气,可能形成光化学烟雾
1.下列不符合当今化学研究方向的是
A.发现新物质 B.合成新材料
C.研究化学反应的微观过程 D.研究化学反应中原子守恒关系
29、(12分)有一份含1 mol HCl和1 mol MgSO4的溶液,当向其中滴加1 mol/L 的Ba(OH)2 溶液时,计算:
(1)当Ba(OH)2 溶液的滴加量到达 L时,开始有氢氧化镁沉淀析出?
(2)当滴加的Ba(OH)2 溶液为1L时,沉淀物的化学式为
每种沉淀物的物质的量为 。
(3)当生成沉淀总质量最大时,Ba(OH)2 溶液的滴加量为 L,此时沉淀的总质量为 g。
 (4)在以下坐标图中绘制出整个过程中产生沉淀的总物质的量(n)与加入 Ba(OH)2
溶液体积(V)之间的关系图。
(4)在以下坐标图中绘制出整个过程中产生沉淀的总物质的量(n)与加入 Ba(OH)2
溶液体积(V)之间的关系图。
28、(本题包括2小题,共14分)
I、(每空2分,共4分)水中若含钙离子(Ca2+)、镁离子(Mg2+)、铁离子(Fe3+)或锰离子(Mn2+),则称为“硬水”,硬水在加热过程中产生沉淀物,不能作为锅炉用水,用作洗涤剂时会降低去污能力,饮用时口感也欠佳。则以Ca2+、Mg2+为主的硬水为例,在水中加消石灰和纯碱的“石灰--纯碱软化法”软化硬水的离子方程式是:
(1)
(2)
Ⅱ、(8分)某一反应体系有反应物和生成物共五种物质:O2 .H2CrO4. Cr(OH)3. H2O H2O2已知该反应中H2O2只发生反应过程: H2O2→O2
(1)、该反应的还原剂是
(2)、该反应的氧化过程是 →
(3)、写出反应的化学方程式并标明电子转移的方向和数目
(4)、如果反应转移了0.3摩电子,则产生的气体在标况下的体积是 升。
27、(16分)右边框图中的物质是中学化学中常见的物质,已知B、E在常温下为气态,其余均为固体,其中D是一种淡黄色固体。试根据框图和所学知识回答下列问题:

(1)写出D的化学式和E的电子式:D的化学式 、E的电子式 。
(2)A+E→C+F的反应方程式为 。
(3)往饱和Na2CO3溶液中不断通入E气体,会看到溶液变浑浊(有白色固体析出),写出该反应的化学方程式 。
(4)将A、D按一定比例投入下图容器的水中,活塞由100mL处上升到200mL处。现用电火花引燃容器内的气体,在条件不变的情况下,若活塞由200mL处回到150mL处,则原则来投入的A、D物质的物质的量之比为n(A)∶n(D)= 。(假设上述操作能顺利实现,且忽略因投入A、D以及气体溶于水使水面高度变化的影响。)

26、(本题包括2小题,共18分)
I、 (10分)在用固体碳酸钠配制500mL 0.1mol/L碳酸钠溶液时,所用到的仪器除天平(含砝码)、烧杯、玻璃棒、胶头滴管外,还需要的仪器是: ;
下述因素使配成的溶液浓度与指定配制浓度相比是:
①偏高 ②偏低 ③无影响
(1) 称量时在托盘天平两边的托盘上放两张大小相同的白纸,然后称取所需碳酸钠固体,倒入烧杯中,用适量蒸馏水溶解_______。(填序号,下同)
(2) 称量时当砝码总和为4g,游码在刻度尺上的读数为0.4g时,天平达到平衡,配制后发现砝码和药品放颠倒了_________。
(3) 溶解碳酸钠时,因加水太多,致使洗涤时用水太少或被迫减少洗涤次数_____。
(4) 溶解碳酸钠所用烧杯不洁净,附有酸性物质________。
(5) 加蒸馏水时,不慎超过了刻度,又用胶头滴管吸出 ______。
(6) 定容时俯视观察液面___________。
(7) 容量瓶用蒸馏水洗净后,未经干燥即用来配溶液___________。
(8) 若所称的碳酸钠中含十水碳酸钠________。
Ⅱ、(8分)随着科学技术的发展,阿佛加德罗常数的测定手段越来越多,测定的精度也越来越高。某同学用下列简单方法测定阿佛加德罗常数,具体步骤为:
①将NaCl固体细粒干燥后,用托盘天平称取m g NaCl固体细粒并转移到100 mL容量瓶中。
②用仪器A向容量瓶中加苯,不断振荡,继续加苯到容量瓶的刻度,计算出NaCl固体的体积V cm3。
 (1)步骤②中仪器A应使用
(填序号)。
(1)步骤②中仪器A应使用
(填序号)。
A.量筒 B.滴管 C.碱式滴定管 D.酸式滴定管
(2) 能否用水代替苯 ,理由是
。
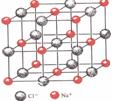
(3) 已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm(如上图),
则用上述方法测得的阿佛加德罗常数NA的表达式为 。
(4) 实验中测得的阿佛加德罗常数与理论值有一定的误差,你认为影响该实验精度的主要原因是
______________________________________________________________。
13、某结晶水合物的化学式为A·nH2O,其相对分子质量为M,在25℃时,a g晶体溶于b g水中即达饱和,形成密度为ρg/mL的溶液,下列表达式正确的是 ( )
A.饱和溶液的物质的量浓度为:1000a(M-18n)/M(a+b)mol/L
B.饱和溶液中溶质的质量分数为:100a(M-18n)/M(a+b)%
C.饱和溶液的体积为:(a+b)/ρL
D.25℃时,A的溶解度为:a(M-18n)/(bM+18an)g
第Ⅱ卷(非选择题,共60分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com