
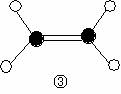
4.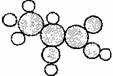 下图是一种有机物的比例模型.该模型代表的有机物可能是
下图是一种有机物的比例模型.该模型代表的有机物可能是
A.饱和一元醇 B.羟基羧酸
C.羧酸酯 D.饱和一元醛
3.生活离不开化学,下列有关说法正确的是
A.乙醇和汽油都是可再生能源.应大力推广使用“乙醇汽油”
B.太阳能电池可采用硅材料制作,其应用有利于环保、节能
C.棉花、蚕丝和人造丝的主要成分都是纤维素
D.凡含有食品添加剂的食物对人体健康均有害,不宜食用
2.下列有关说法或判断正确的是
A.H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体
B.乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能为同分异物体
C.HI的相对分子质量大于HF,所以HI的沸点高于HF
D.离子化合物中可能含共价键,但共价化合物中不含离子键
1.查阅资料发现,金属钠不仅能跟氧气和水反应.还能跟多种其它物质发生反应,其中包括与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与水反应的异同点, 下列的研究方法中没有用到的是
A.实验法 B.观察法 C.分类法 D.比较法
21.(有机化学基础模块,10分)
已知烃A不能使溴水褪色,A的相对分子质量为106,它在NMR(核磁共振)图谱中有两个信号。A在一定条件下可以发生下列转化:

请回答下列问题:
(1)A结构简式 ;反应②的条件 ;
反应①的反应类型 。
(2)写出反应③的化学方程式: .
(3)F在浓硫酸加热条件下反应得到的产物是一种气体,请写出与该气体属于同类物质的所有可能的同分异构体的结构简式(包括顺反异构): 。
20.(物质结构与性质模块,10分)
有A、B、C、D、E五种元素,其中A、B、C、D为短周期元素,A元素的周期数、主族数、原子序数相同;B原子核外有3种能量不同的原子轨道且每种轨道中的电子数相同;C原子的价电子构型为csc cpc+1,D元素的原子最外层电子数比次外层电子数少2个,D的阴离子与E的阳离子电子层结构相同,D和E可形成化合物E2D。
(1)上述元素中,第一电离能最小的元素的原子结构示意图为 ;D的电子排布式为 ;
(2)下列分子结构图中的 和
和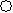 表示上述元素的原子中除去最外层电子的剩余部分,
小黑点表示没有形成共价键的最外层电子,短线表示共价键。
表示上述元素的原子中除去最外层电子的剩余部分,
小黑点表示没有形成共价键的最外层电子,短线表示共价键。
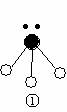
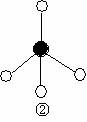

则在以上分子中,中心原子采用sp3杂化形成化学键的是 (填写分子的化学式); 在③的分子中有 个σ键和 个π键。
(3)A、C、D可形成既具有离子键又具有共价键的化合物,其化学式可能为 ;C的氢化物水溶液与足量AgNO3 溶液反应生成的配合物,其化学式为 ,请说出该配合物中中心原子与配位体及内界与外界之间的成键情况:
。
19.(化学与技术模块,10分)
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上使用的“海水淡化”主要技术有 。
(2)工业上利用电解饱和食盐水可制得重要化工产品,用离子交换膜电解槽电解饱和食盐水,反应的离子方程式是 ,阳离子交换膜的作用是 。若不使用离子交换膜法电解食盐水,可得到一种消毒液,其反应的化学方程式是 。
(3)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,写出此过程中SO2 被吸收以及又生成可被回收的气体的两个反应的化学方程式 。
18.(化学与生活模块,10分)
化学与我们的生活息息相关,合理使用化学物质,提高生活质量是应引起我们关注的问题。请回答下列问题:
(1)1989年世界卫生组织把铝列为食品污染物之一,一个成年人每日摄入量应控制在4mg以下,因铝元素含量较多会引发人体患老年性痴呆。铝在下列应用时应加以控制的是
①制铝合金 ②制电线 ③制炊具 ④明矾净水 ⑤明矾与苏打制食品膨松剂 ⑥用氢氧化铝凝胶制胃舒平药片 ⑦制银白色油漆 ⑧铝制易拉罐 ⑨用铝箔包装糖果和小食品。
(2)随着人们生活水平的提高,居室装修成为大众时尚,但居室污染也成为主要的健康杀手之一。室内装修材料释放出的有毒气体主要是 ,建筑石材放射出的有害气体主要是 ,这二者都会对人体健康造成严重威胁,如引发癌症等。
(3)铁是人体必须的微量元素之一,当铁的摄入量不足时,可能会导致缺铁性贫血,对于缺铁人群可以服用补铁剂或补铁保健品。下列可以作为补铁剂的是 (填字母序号)。
A.硫酸亚铁 B.硫酸铁 C.葡萄糖酸亚铁 D.乳酸亚铁
设计实验检验某补铁保健品中是否含有铁,写出实验步骤、现象、结论和相关反应的离子方程式。
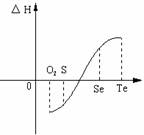
17.(10分)某化学兴趣小组,专门研究了氧族元素及其某些化合物的部分性质。所查资料如下:
(1)碲(Te)为固体,H2Te为气体,Te和H2不能直接化合生成H2Te
(2)等物质的量氧气、硫、硒、碲与H2反应的焓变情况如图所示:
请回答下列问题:
(1)H2与硫化合的反应 热量(填“放出”或“吸收”)。
(2)已知H2Te分解反应的△S>0,请解释为什么Te和H2不能直接化合
。
(3)H2S的水溶液显弱酸性,写出其电离方程式 ;在一定温度下,它的第一级电离常数可用 Ka表示,Ka 值越大,表示_________,Ka值大小与温度的关系是:温度升高,Ka 值_________(填一定增大、一定减小、或可能增大也可能减小)。
(4)在容积均为1 L(容器体积不可变)的甲、乙两个容器中,分别加入2 mol SO2、
1 mol O2 和4 mol SO2、2 mol O2,在相同温度、催化剂下使其反应。最终达到平衡后,两容器中SO2转化率分别为α 甲、α 乙,甲容器中平衡常数表达式为 ,此时α 甲 α 乙(填“大于”、“小于”或“等于”)。
第Ⅲ卷 非选择题(选做)
(包括4小题,每小题10分。考生最多可从中选做2小题,若多选作,按照模块呈现的顺序首先作答的计分。满分20分)
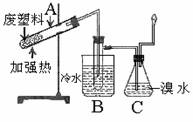
16.(6分) 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图。
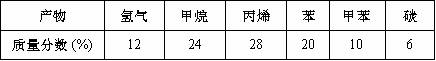
加热某废塑料得到的产物如下表所示:
回答下列问题:
(1)上述处理废旧塑料的方法为
A.蒸馏 B.干馏 C.高温灼烧 D.加聚
(2)你认为生产该塑料的单体是
A.甲烷 B.丙烯 C.氢气 D.苯
(3)装置C中盛溴水的仪器名称为 ,实验过程中在该仪器中观察到的现象 。
(4)取装置B试管中收集到的液体加入溴水振荡后静置,观察到的现象为
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com