
18.(7分)
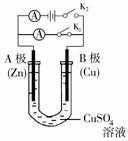
如右图所示,请按要求回答下列问题。
(1)打开K ,合并K
,合并K 。
。
A为(填“正”或“负”)_______极,在该电极可观察到的现象是____________________;B极的电极反应为____________________。
(2)打开K ,合并K
,合并K 。
。
A为(填“阴”或“阳”)_______极,在该电极可观察到的现象是__________________;B极的电极反应为_______________;当有0.2mol电子转移时,则析出铜的质量为_____g。
17.(6分)
现有一瓶浓度为0.2mol/L某酸溶液,可能为醋酸、盐酸或硫酸中的一种。为了确定该酸溶液的组成进行实验:取20.00mL该酸溶液,逐滴加入0.2mol/L的氢氧化钠溶液,恰好完全反应时所需碱液体积20.00mL。请回答下列问题。
(1)该酸不可能是______________;
(2)用pH试纸测得反应后所得溶液呈碱性,根据此现象说明该酸溶液为_______________;用离子方程式说明溶液呈碱性的原因_________________________;
(3)反应后所得溶液中离子浓度由大到小的顺序是__________________________。
16.(6分)
某校课外小组同学制备Fe(OH)3胶体,并研究该胶体的性质。
(1)该小组同学采用了以下操作制备胶体,请将空白处填写完整。
 取一个烧杯,加入20mL蒸馏水,加热至沸腾,然后向烧杯中滴加1mL-2mL饱和__________溶液,继续煮沸,待_________后,停止加热;
取一个烧杯,加入20mL蒸馏水,加热至沸腾,然后向烧杯中滴加1mL-2mL饱和__________溶液,继续煮沸,待_________后,停止加热;
(2)将制得的胶体放入半透膜制成的袋内,如右图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察(填写“有”或“无”)_________ 丁达尔现象:再向试管中加入用稀硝酸化的硝酸银溶液,可观察到的现象为______________________________;
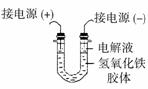 (3)将半透膜内的液体倒入U 型管中,如右图所示,在液体上方加入少量电解液以保护胶体,接通直流电后,观察到的现象是(填“阴”或“阳”)________极附近颜色逐渐变深,其原因是________________________________________________________。
(3)将半透膜内的液体倒入U 型管中,如右图所示,在液体上方加入少量电解液以保护胶体,接通直流电后,观察到的现象是(填“阴”或“阳”)________极附近颜色逐渐变深,其原因是________________________________________________________。
15.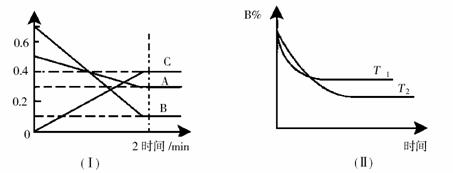 T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B和C物质的量变化与时间关系如下图(Ⅰ)所示。若保持其它条件不变,温度分别为T
T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B和C物质的量变化与时间关系如下图(Ⅰ)所示。若保持其它条件不变,温度分别为T 和T
和T 时,B的物质的量分数与时间关系如下图(Ⅱ)所示。下列叙述正确的是
时,B的物质的量分数与时间关系如下图(Ⅱ)所示。下列叙述正确的是
A.2min内A的化学反应速率为0.1mol/L
B.在反应达到平衡时,保持其它条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动
C.在反应达到平衡时,保持其它条件不变,升高温度,正逆反应速率都增大,且A的转化率增大
D.在T℃时,若A的浓度减少了1mol/L,则B的浓度会减少3mol/L,C的浓度会增加2mol/L
第Ⅱ卷(非选择题 共55分)
14.25℃时,在100g质量分数为10%的X溶液中加入5gX(无水盐)后,恰好达到饱和,则25℃时X的溶解度为
A.10.0g B.15.0g C.16.7g D.18.8g
13.燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如右图所示,a、b均为惰性电极。下列叙述不正确的是
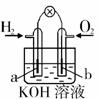 A.a极是负极,该电极上发生氧化反应
A.a极是负极,该电极上发生氧化反应
B.b极反应是O +4OH
+4OH -4e
-4e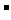 =2H
=2H O
O
C.总反应方程式为2H +O
+O =2H
=2H O
O
D.氢氧燃料电池是一种具有应用前景的绿色电源
12.常温下,一定体积pH=3的二元弱酸H R溶液与一定体积pH=11的NaOH溶液混合后溶液呈中性。下列断判正确的是
R溶液与一定体积pH=11的NaOH溶液混合后溶液呈中性。下列断判正确的是
A.溶液中c(Na )=10
)=10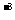 mol/L
mol/L
B.溶液中c(R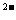 )>c(Na
)>c(Na )>c(H
)>c(H )>c(OH
)>c(OH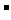 )
)
C.溶液中c(R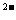 )+c(OH
)+c(OH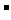 )+c(HR
)+c(HR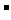 )=c(Na
)=c(Na )+c(H
)+c(H )
)
D.溶液中2c(R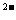 )+c(HR
)+c(HR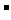 )=c(Na
)=c(Na )
)
11.设N 为阿德罗常数。下列说法正确的是
为阿德罗常数。下列说法正确的是
A.2 L 1mol/L NH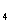 Cl溶液含NH
Cl溶液含NH 和Cl
和Cl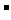 均为2 N
均为2 N
B.在常温常压下,22g二氧化碳含有共有电子对总数为2 N
C.0.1 molOH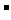 的质子数与0.1molH
的质子数与0.1molH O的电子数均为N
O的电子数均为N
D.在标准状况下,11.2L辛烷中的碳原子数为4 N
10.下列离子方程式中,正确的是
A.碳酸钙与盐酸混合2H +CO
+CO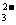 =CO
=CO ↑+H
↑+H O
O
B.向氯化铁溶液中加入铁粉Fe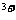 +Fe=2Fe
+Fe=2Fe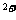
C.亚硫酸钠溶液与稀硫酸混合2H +SO
+SO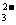 =SO
=SO ↑+H
↑+H O
O
D.二氧化锰与浓盐酸混合后加热MnO +4H
+4H +4Cl
+4Cl =MnCl
=MnCl +Cl
+Cl ↑+2H
↑+2H O
O
9.下列各组离子中,在无透明的酸性溶液中,可以大量共存的是
A.Al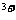 、Na
、Na 、SO
、SO 、Br
、Br B.Na
B.Na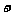 、NH
、NH 、NO
、NO 、I
、I
C.K Mg
Mg 、Fe
、Fe 、Cl
、Cl D.Na
D.Na 、AlO
、AlO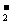 、SO
、SO 、CO
、CO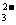
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com