
9.对溶液中的离子进行鉴定,下列实验所得结论不合理的是
A.溶液中加入稀硝酸后,再加入AgNO3溶液,有白色沉淀生成,则说明溶液中含有Cl-
B.溶液中加入KSCN溶液,无红色出现,继续加入氯水,溶液变红,说明溶液中一定含有Fe2+
C.溶液中加入NaOH溶液,加入后产生使湿润的红色石蕊试纸变蓝的气体,则可推断该溶液中含有NH4+
D.向溶液中加入盐酸,有使澄清石灰水变浑浊的无色无味的气体放出,可推测溶液中含有CO32-
8.下列解析中,不科学的是
A.“水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用生成了可溶性Ca(HCO3)2
的缘故
B.长期盛放NaOH溶液的滴瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气体减少形成“负压”的缘故
C.严格地讲,“通风橱”是一种不负责任地防污染手段,因为实验产生地有害气体没有得到转化或吸收
D.“雨后彩虹”“海市蜃楼”既是一种自然现象又是光学现象,也与胶体的知识有关
7.已知1-18号元素离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是
A.质子数:c>d B.离子的还原性:Y2->Z-
C.氢化物的稳定性:H2Y>HZ D.原子半径:X<W
6.设NA为阿伏加德罗常数的值,下列叙述正确的是
A.1L1mol•L-1醋酸溶液中离子总数为2NA
B.5.6g铁与足量盐酸反应转移的电子数为0.3NA
C.3.5g35Cl2气体在标准状况下的体积为22.4L
D.20g重水(2H2O)中含有的中子数为10NA
4.近期《美国化学会志》报道,中国科学家以二氧化碳位碳源,金属钠为还原剂,在470℃、80Mpa下合成出金刚石,具有深远意义。下列说法不正确的是
A.金刚石是碳元素的一种同素异形体
B.金刚石在空气中完全燃烧只生成CO2
C.由CO2合成金刚石是物理变化
D.CO2中的碳元素为化合态,而金刚石中碳元素为游离态
|
|
①CaBr2+H2O=======CaO+2HBr ②2HBr+Hg=======HgBr2+H2
|
|
③HgBr2+CaO======HgO+CaBr2
④HgO======Hg+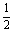 O2
O2
但这些设想如何进一步操作尚未解决,这种联合反应的目的是为了制备
A. H2 B. HBr C.CaO D.Hg
3.日常生活中,下列做法错误的是
A.用燃烧法区别毛织品和棉织品 B.用蒸发法区别蒸馏水和自来水
C.用闻气味的方法区别酒精和食醋 D.用淀粉溶液区别含碘盐和不含碘盐
2.金属钠不仅能跟水反应,也能与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与水和氧气反应的异同点,下列的研究方法用不着的是
A.分类法 B.实验法 C.观察法 D.比较法
1.下列关于化学反应的说法,错误的是
A.化学反应都有新物质生成 B.化学反应都伴随着能量的变化
C.化学反应都是可逆反应 D.化学反应的实质就是旧键断裂,新键形成
24.(8分)使一定量的H2在Cl2中充分燃烧,将反应后的气体缓慢通入100ml 1.0mol·L-1的NaOH溶液中。下图甲表示某种离子的物质的量(n)随通入气体体积(V)的变化曲线;图乙表示溶液的导电性随通入气体体积(V)的变化曲线。
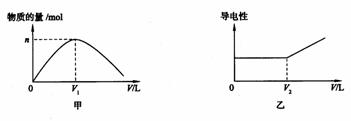
请回答下列问题:
(1)图甲表示溶液中 离子的变化曲线。(填写下列各项的序号)
①H+ ②Na+ ③Cl- ④ClO-
(2)图乙中,当通入的气体体积大于V2时,引起溶液导电性明显增强的主要阴、阳离子是 和 (填写离子符号)。
(3)设n=0.01mol, 试确定点燃前H2和Cl2的物质的量之比(写出计算过程)。
23.(11分)X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如下图所示变化:
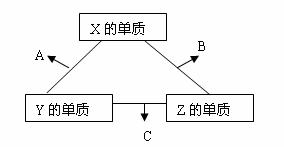
已知一个B分子中含有的Z元素的原子个数比C分子中的少一个。
请回答下列问题:
(1)X元素在周期表中的位置是 。
(2)X的单质与Z的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入 (填物质名称);负极电极反应式为 。
(3)C在一定条件下反应生成A的化学方程式是 。
(4)X、Y、Z三种元素可组成一种强酸,W,C在适当条件下被W溶液吸收生成一种盐。该盐的水溶液pH 7(填“大于”、“小于”或“等于”)其原因是(用离子方程式表示): 。
(5)已知Y的单质与Z的单质生成C的反应是可逆反应,△H<0。将等物质的量的Y、Z的单质充入一密闭容器中,在适当催化剂和恒温,恒压条件下反应。下列说法中,正确的是 。(填写下列各项的序号)
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y的单质的体积分数始终为50%
c.达到化学平衡时,Y、Z的两种单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中,混合气体平均相对分子质量减小
e.达到化学平衡后,再升高温度,C的体积分数增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com