
9£®ŌŚŅ»ĆܱÕČŻĘ÷ÖŠ£¬·“Ó¦aA(g)bB(g)“ļĘ½ŗāŗ󣬱£³ÖĪĀ¶Č²»±ä£¬½«ČŻĘ÷ČŻ»żŌö¼Ó
Ņ»±¶£¬“ļµ½ŠĀĘ½ŗāŹ±£¬BµÄÅØ¶ČŹĒŌĄ“µÄ60%”£ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ
””.. A£®a£¾b”””””””””””””” ””””””””””””B£®Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆĮĖ
... C£®AµÄ×Ŗ»ÆĀŹ¼õŠ”ĮĖ”””””””””””””” D£®BµÄÖŹĮæ·ÖŹż¼õŠ”ĮĖ
8£®X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪµŻŌöµÄČżÖÖ¶ĢÖÜĘŚŌŖĖŲ”£XŌ×ӵĵē×Ó²ćŹżÓėĖüµÄŗĖĶāµē×Ó×ÜŹżĻąĶ¬£¬¶ųZŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄČż±¶£¬YŗĶZæÉŅŌŠĪ³ÉĮ½ÖÖŅŌÉĻĘųĢ¬»ÆŗĻĪļ”£ŌņĻĀĮŠĖµ·ØŅ»¶ØÕżČ·µÄŹĒ
A£®ĘäÖŠÓŠĮņŌŖĖŲ”””””””””””””””” B£®ĘäÖŠÓŠ½šŹōŌŖĖŲ
C£®ÕāČżÖÖŌŖĖŲÄܹ»×é³ÉŃĪ”””” ”””” D£®ÕāČżÖÖŌŖĖŲ¾łĪ»ÓŚ²»Ķ¬ÖÜĘŚ
7£®ŅŃÖŖ1-18ŗÅŌŖĖŲµÄĄė×ÓaW3+”¢bX+”¢cY2£”¢dZ£¶¼¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬ĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ
A£®Ąė×ӵĻ¹ŌŠŌ£ŗY2££¾Z£”””””””””””” B£®ÖŹ×ÓŹż£ŗc£¾b ””
C£®Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗH2Y£¾HZ”””””””””” D£®Ō×Ó°ė¾¶£ŗX£¼W””
6£®Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚÄ³¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśæÉÄę·“Ó¦A(g)+3B(g)2C(g)£¬ÄÜ
±źÖ¾øĆ·“Ó¦“ļµ½Ę½ŗāµÄŹĒ
A£®A”¢B”¢CµÄÅضČÖ®±ČĪŖ1”Ć3”Ć2””””””
B£®µ„Ī»Ź±¼äÄŚÉś³Én molAµÄĶ¬Ź±Éś³É3n molB””””””””””””
C£®µ„Ī»Ź±¼äÄŚÉś³Én molAµÄĶ¬Ź±Éś³É2n molC””””””””””””
D£®»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä
5£®ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A£®ŌŚÖŠŗĶµĪ¶ØÖŠ£¬¼ČæÉÓƱź×¼ČÜŅŗµĪ¶Ø“ż²āČÜŅŗ£¬Ņ²æÉÓĆ“ż²āČÜŅŗµĪ¶Ø±ź×¼ČÜŅŗ
B£®½ųŠŠÖŠŗĶµĪ¶Ø²Ł×÷Ź±£¬ŃŪ¾¦ŅŖŹ¼ÖÕ×¢ŹÓµĪ¶Ø¹ÜÄŚČÜŅŗŅŗĆęµÄ±ä»Æ””””
C£®²ā¶ØÖŠŗĶČČŹ±£¬Į½ÉÕ±¼äĢīĀśĖéÖ½µÄ×÷ÓĆŹĒ¹Ģ¶ØŠ”ÉÕ±
D£®ČōÓĆ50mL 0.55mo1”¤L-1µÄĒāŃõ»ÆÄĘČÜŅŗ£¬·Ö±šÓė50mL 0.50mo1”¤L-1µÄŃĪĖįŗĶ50mL 0.50mo1”¤L-1µÄĮņĖį·“Ó¦³ä·Ö·“Ó¦£¬Į½·“Ó¦µÄÖŠŗĶČČ²»ĻąµČ
4£®¶ŌÓŚ»Æѧ·“Ó¦ÄÜ·ń×Ō·¢½ųŠŠ£¬ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ
A£®Čō¦¤H£¼0£¬¦¤S£¾0£¬ČĪŗĪĪĀ¶ČĻĀ¶¼ÄÜ×Ō·¢½ųŠŠ””””””””””
B£®Čō¦¤H£¾0£¬¦¤S£¼0£¬ČĪŗĪĪĀ¶ČĻĀ¶¼²»ÄÜ×Ō·¢½ųŠŠ””””””””
C£®Čō¦¤H£¾0£¬¦¤S£¾0£¬µĶĪĀŹ±æÉ×Ō·¢½ųŠŠ””””””””””””””””
D£®Čō¦¤H£¼0£¬¦¤S£¼0£¬µĶĪĀŹ±æÉ×Ō·¢½ųŠŠ””””””””””””””””
3£®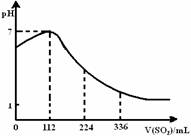 ijĶ¬Ń§Ļņ100mLĒāĮņĖįČÜŅŗÖŠĶØČĖ±ź×¼×“æöĻĀµÄ¶žŃõ»ÆĮņĘųĢ壬ĖłµĆČÜŅŗpH±ä»ÆČēĶ¼Ėł”£Ėū¾Ż“ĖµĆµ½µÄĻĀĮŠĖÄĢõ¹ŲÓŚ¶žŃõ»ÆĮņŗĶŃĒĮņĖįµÄĖµ·Ø”£Ēė·ÖĪöĘäÖŠÕżČ·µÄŹĒ
ijĶ¬Ń§Ļņ100mLĒāĮņĖįČÜŅŗÖŠĶØČĖ±ź×¼×“æöĻĀµÄ¶žŃõ»ÆĮņĘųĢ壬ĖłµĆČÜŅŗpH±ä»ÆČēĶ¼Ėł”£Ėū¾Ż“ĖµĆµ½µÄĻĀĮŠĖÄĢõ¹ŲÓŚ¶žŃõ»ÆĮņŗĶŃĒĮņĖįµÄĖµ·Ø”£Ēė·ÖĪöĘäÖŠÕżČ·µÄŹĒ
A£®SO2 ŹĒČõµē½āÖŹ ”””””””””””””””””” ””
B£®H2SO3²»ŹĒĒæĖį””””
C£®ŃĒĮņĖįŹĒ±ČĒāĮņĖį»¹ČõµÄĖį
D£®ŌĒāĮņĖįČÜŅŗµÄĪļÖŹµÄĮæÅضČ0.05mo1”¤L-1
2£®ĻÖÓĆĀČĖ®Ą“ÖĘČ”ŗ¬ÓŠ“ĪĀČĖįµÄČÜŅŗ£¬¼ČŅŖĢįøßČÜŅŗÖŠHClOĪļÖŹµÄĮæÅØ¶Č£¬ÓÖŅŖ½µµĶČÜŅŗÖŠHClÅØ¶Č£¬ĻĀĮŠ“ėŹ©æÉŅŌ²ÉÓƵďĒ
A£®¼ÓČȻӷ¢HCl”” ”””””””””””””” B£®¼ÓĖ®Ź¹Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
C£®¼ÓNaOHÖŠŗĶHCl”” ”””””””””””” D£®¼ÓCaCO3 ÖŠŗĶHCl””
1£®ĻņĖ®ÖŠ¼ÓČėĻĀĮŠĪļÖŹ£¬ĘäÖŠÄÜŹ¹Ė®µÄµēĄė³Ģ¶ČŌö“óµÄĪļÖŹŹĒ
””A£®NaCl ”””””””” ””B£®NH4Cl”””””””””” C£®HCl”””””””””””” D£®NaOH
26”¢ĪŅ¹ś²ĪÓėŃŠÖʵİ¢¶ū·Ø“ÅĘ×ŅĒĖęĆĄ¹ś·¢ĻÖŗÅŗ½Ģģ·É»śÉżČėĢ«æÕ£¬Ģ½Ė÷ÓīÖęÖŠŹĒ·ń“ęŌŚ”°·“ĪļÖŹ”±(ÓÖ³ĘĪŖ”°°µĪļÖŹ”±)µÄŃŠ¾æ¹¤×÷”£”°·“ĪļÖŹ”±µÄÖ÷ŅŖĢŲÕ÷ŹĒµē×Ó“ųÕżµēŗÉ£¬ÖŹ×Ó“ųøŗµēŗÉ”£ĪļÖŹŗĶĘäĻąÓ¦µÄ·“ĪļÖŹĻąÓöŗó·¢ÉśäĪĆš£¬ĖłÓŠµÄÖŹĮæĶźČ«×Ŗ»ÆĪŖÄÜĮ攣ÓĆÉĻŹöŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ
””(1)øł¾ŻÄćĖłŃ§¹żµÄÖŖŹ¶ĶĘ²āÖĘŌģ°¢¶ū·Ø“ÅĘ×ŅĒŗĖŠÄ²æ¼žµÄ²ÄĮĻŹĒĻĀĮŠÄÄŅ»ÖÖ?
”””””” A”¢FeO”””” B”¢Fe2O3.”””” C”¢Fe3O4”””” D”¢ Fe3C
””(2)·“ĪļÖŹÖŠŗĶ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ
”””””” A”¢H- + OH+===H2O”””” B”¢H+ + OH+====H2O
C”¢H- + OH-==H2O”””””” D”¢H+ + OH-====H2O
(3)»³öĒāĄė×ӵķ“ĪļÖŹŌ×Ó½į¹¹Ź¾ŅāĶ¼”£
(4)¼ĘĖć1gĒāĄė×ÓŗĶ1g·“ĒāĄė×Ó·¢ÉśäĪ Ćš(ÖŹĮæ±äĪŖÄÜĮæ)ŗó·Å³öÄÜĮæĪŖ¶ąÉŁ½¹£æ
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com