
19.(8分)现有常温下的0.1mol·L-1纯碱溶液。
(1)你认为该溶液呈碱性的原因是(用离子方程式表示): ①
为证明你的上述观点,请设计一个简单的实验,简述实验过程: ②
(2)同学甲认为该溶液中Na2CO3的水解是微弱的,发生水解的CO2-3 离子不超过其总量的10%。请你设计实验证明该同学的观点是否正确。 ③
(3)同学乙就该溶液中粒子之间的关系写出了下列四个关系式,你认为其中正确的是
④
A.c(Na+)=2c(CO2-3 ) B.c(CO2-3 )>c(OH-)>c(HCO-3)>c(H2CO3)
C.c(CO2-3 )+c(HCO-3)=0.1mol·L-1 D.c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3)
(4)水解反应是典型的可逆反应。水解反应的化学平衡常数称为水解常数(用Kh表示),
请写出Na2CO3第一步水解反应的水解常数的表示式: ⑤
18.(8分)已知水在25℃和95℃时,其电离平衡曲线如右图所示:
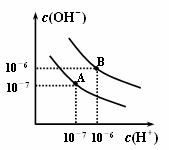
(1)则25 时水的电离平衡曲线应为 ①
(填“A”或“B”),请说明理由 ②
(2)25时,将=9的NaOH溶液与=4的溶液混合,
若所得混合溶液的 =7,则NaOH溶液与溶液的体积比为 ③
(3)95时,若100体积1=的某强酸溶液与1体积2=b的某强碱溶液混合后
溶液呈中性,则混合前,该强酸的1与强碱的2之间应满足的关系是 ④
(4)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合
后,混合溶液的pH=5。请分析其原因: ⑤
17.(8分)将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要化学反应为:C+H2O(g)高温CO+H2。
C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1;
H2(g)+O2(g)=H2O(g) △H2=-242.0kJ·mol-1;
CO(g)+O2(g)=CO2(g) △H3=-283.0kJ·mol-1;
试回答:
(1)请你根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式: ①
(2)比较反应热数据可知,1molCO(g)和1 molH2(g)完全燃烧放出的热量之和,比
1molC(s)完全燃烧放出的热量 ② (填“多”或“少”)。
甲同学据此认为:“煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量。”
乙同学根据盖斯定律作出了下列循环图
 C(s)+H2O(g)+O2(g)
△H1CO2(g)+H2O(g)
C(s)+H2O(g)+O2(g)
△H1CO2(g)+H2O(g)
CO(g)+O2(g)+H2(g) △H3CO(g)+H2O(g)+O2(g)
请你写出△H1、△H2、△H3、△H4之间存在的关系式 ③
乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同。”请分析:甲、乙两同学观点正确的是 ④ (填甲或乙)同学,另一同学出现错误观点的原因是 ⑤
16.举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂。有一种兴奋剂的结
构简式如右式,下列有关该物质的说法正确的是
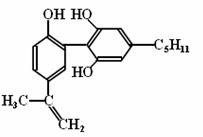
A.该分子中所有碳原子可以稳定的共存在一个平面中
B.1mol该物质与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为4mol、7mol
C.遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物
D.滴入酸性KMnO4溶液,观察到紫色褪去,可证明分子中存在双键
第II卷 (非选择题 共64分)
15.在阿斯匹林的结构简式(右式)中①②③④⑤⑥分别标出了其分子中的不同的键。将阿斯匹林与足量NaOH溶液共煮时,发生反应时断键的位置是
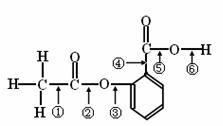
A.①④ B.②⑤ C.③④ D.②⑥
14.已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是
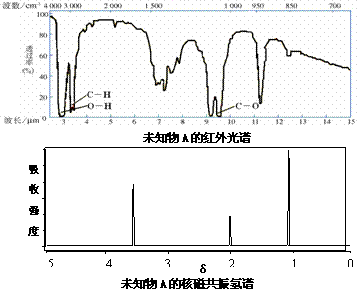
A.由红外光谱可知,该有机物中至少含有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1:2:3
C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3-O-CH3
13.氨气溶于水时,大部分NH3与H2O以氢键(用“···”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为
A.… B.H-…H- C.H-… D.…H-
《有机化学基础》模块选择题
12.下列说法错误的是
A.O3与SO2的结构与性质相似
B.硫粉不溶于水易溶于CS2中
C.Be(OH)2是两性氢氧化物
D.在相同条件下, 的沸点高于
《物质结构与性质》模块选择题
11.下列性质不能用金属键理论解释的是
A.导电性 B.导热性 C.延展性 D.锈蚀性
10.已知Ksp(AgCl )=1.8×10-10,Ksp(AgI)=1.0×10-16。下列关于不溶物之间转化的
说法中错误的是
A.AgCl不溶于水,不能转化为AgI
B.两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物
C.AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于
×10-11 mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com