
10.向一定浓度的下列物质澄清溶液中通入过量的CO2气体,最后肯定没有沉淀生成的是( )
①Ca(OH)2 ②Na2CO3 ③CaCl2 ④Ca(ClO)2
A.①③④ B.②③④ C.①②③ D.①②③④
9.用NA表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.4 g重水(D2O)中所含质子数为0.2 NA
B.4.48 L N2与CO的混合物所含分子数为0.2 NA
C.6.2 g白磷与红磷的混合物中所含磷原子数为0.2 NA
D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2 NA
8.硝酸铵在不同条件下分解可以得到不同的产物,下列各组物质中肯定不可能是硝酸铵分
解产物的是 ( )
A.N2O、H2O B.N2、O2、H2O
C.N2、HNO3、H2O D.NH3、NO、H2
7.物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,已知溶液中的c(H+)<c(OH-),
下列关系式正确的是 ( )
A.c(CN-)>c(Na+) B.c(HCN)<c(CN-)
C.c(CN-)+ c(OH-)=0.1mol·L-1 D. c(HCN)+ c(CN-)=0.2mol·L-1
6.下列叙述正确的是 ( )
A.室温时10mL 0.02mol·L-1 HCl溶液与10mL 0.02mol·L-1 Ba(OH)2溶液充分混合,
若混合后溶液的体积为20mL,则溶液的pH=12
B.0.1mol·L-1氨水中, c(OH-)<c(NH4+)< 0.1mol
C.在0.1mol·L-1 CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)-C(CH3COO-)
D.0.1mol·L-1某二元弱酸碱性NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
5.一定能在下列溶液中大量共存的离子组是 ( )
A.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl-
B.c(H+)=1×10-13mol·L-1的溶液:Na+、Ca2+、SO42-、CO32-
C.含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-
D.含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl-
4.空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民
的支持。下列措施不利于“蓝天工程”建设的是 ( )
|
B.加大石油、煤炭的开采速度,增加化石燃料的供应量
C.研制开发燃料电池汽车,消除机动车尾气污染
D.实施绿化工程,防治扬尘污染
3.下列说法或表示法正确的是 ( )
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)→C(金刚石):ΔH = +119 kJ· mol-1可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-aq)-===H2O(l);ΔH=-57.3 kJ· mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l);ΔH=-285.8 kJ· mol-1
2.下列各对应反应的离子方程式正确的是 ( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
B.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-=Cl2↑+Mn2++H2O
C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
D.用可溶性铝盐溶液和过量氢氧化钠溶液制取氢氧化铝:Al3++3OH-=Al(OH)3↓
1.一定温度下,有可逆反应:2A(g)+2B(g) C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。( )
C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。( )

|
关于两容器中反应的说法正确的是
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,但混合气]
体的平均相对分子质量不相同
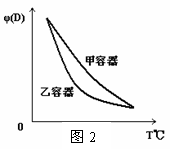
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2 所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com