
1.空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”建设的是( )
A.推广使用燃煤脱硫技术,防治SO2污染
B.实施绿化工程,防治扬尘污染
C.研制开发燃料电池汽车,消除机动车尾气污染
D.加大石油、煤炭的开采速度,增加化石燃料的供应量
24.(6分)两种烃的衍生物A和B,所含碳、氢、氧的质量比均为6:1:4。完全燃烧0.1molA能生成3.6g水。B只含一个醛基,1.1gB与足量银氨溶液反应,可析出2.7gAg
(1)求 A和B的分子式,
(2)若B能与酸发生酯化反应,且主链含3个碳原子,写出其可能的结构简式。
23.(3分)某烃的含氧衍生物A的相对分子质量为240,其碳的质量分数为80.0%,氧的质量分数是氢的质量分数的2倍,分子中含有2个苯环,每个苯环上都只有一个取代基,该取代基无支链。A在稀酸溶液中加热时发生水解,得到B和C,C的相对分子质量为108。请写出:
(1)A的分子式 ▲ 。(2)C的结构简式 ▲ 。(3)B的结构简式 ▲
22.(14分)
苏丹红一号(sudan I)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2-萘酚为主要原料斜备的,它们的结构简式如下所示:
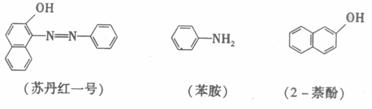
(1)苏丹红一号的化学式(分子式)为 ▲
(2)在下面化合物(A)~(D)中,与2-萘酚互为同分异构体的有(填字母代号) ▲
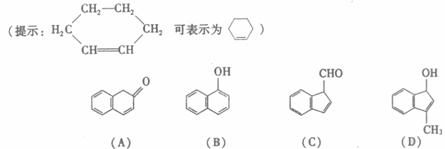
(3)上述化合物(C)含有的官能团是 ▲
(4)在适当的条件下,2-萘酚经反应可得到芳香化合物E(C8H6O4),1mol E与适量的碳酸氢钠溶液反应可放出二氧化碳44.8 L(标准状况),E与溴在有催化剂存在时反应只能生成两种一溴取代物,两种一溴取代物的结构简式分别是 ▲ ,E与碳酸氢钠反应的化学方程式是 ▲
(5)若将E与足量乙醇在浓硫酸作用下加热,可以生成一个化学式(分子式)为C12H14O4的新化合物,该反应的化学方程式是 ▲ 反应类型是 ▲ 。
21.(6分)A、B、C、D、E五种有机物,它们的分子分别由-CH3、-OH、-COOH、-C6H5、-CHO中的两种组成,这些化合物的性质如下所述:
(1)A能够发生银镜反应,且相对分子质量为44;
(2)B溶液加入氯化铁溶液中,溶液显紫色;
(3)C和E在有浓硫酸存在并加热的条件下,能发生酯化反应,C和E的相对分子质量之比为8:15;
(4)B和E都能跟氢氧化钠溶液反应,而A、C、D则不能;
(5)D能使酸性高锰酸钾溶液褪色,还能发生硝化反应。
由此可知, C、D、E的结构简式是: C ▲ D ▲ E ▲ 。
20.(11分)某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质,首先做了银镜反应.
(1)在甲酸进行银镜反应前,必须在其中加入一定量的 ▲ ,因为 ▲ .
(2)写出甲酸进行银镜反应的化学方程式 ▲ .
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作 ▲ (写字母):
A、用洁净的试管;
B、在浓度为2%的NH3·H2O中滴入稍过量的浓度为2%的硝酸银;
C、用前几天配制好的银氨溶液;
D、在银氨溶液里加入稍过量的甲酸;
E、用小火对试管直接加热;
F、反应过程中,振荡试管使之充分反应.
然后,同学们对甲酸与甲醇进行了酯化反应的研究:
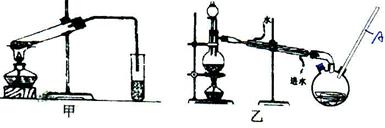
(4)乙装置中长导管A的作用是 ▲
(5)写出甲酸和甲醇进行酯化反应的化学方程式 ▲
(6)选择甲装置还是乙装置好? ▲ ,原因是 ▲ .
(7)实验过程中选用的药品及试剂有:浓H2SO4、甲醇、甲酸还有 ▲ 、
▲ 两种必备用品.
(8)一同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释 ▲
19.(8分)A、B、C、D、E、F是常见单质,其中A是用量最大,应用最广泛的金属;元素D是地壳中含量最多的金属元素;D元素和E元素在周期表中相邻。G、H、I、J、K、L是常见化合物,其中G在常温下是无色液体,H是黑色固体。以上物质相互间的转化关系如下图所示:
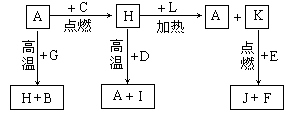
请回答下列问题:
(1)元素A在元素周期表中的位置为 ▲ 周期 ▲ 族。
(2)写出K的电子式 ▲ 。
(3)写出H和D反应的化学方程式 ▲ 。
(4)D能与氢氧化钠溶液反应,请写出该反应的离子方程式 ▲ 。
(5)写出A与G反应的化学方程式 ▲ 。
(6)K与E反应时产生的现象有 ▲ ;
该反应的化学方程式为 ▲ 。
18.(4分)短周期元素X、Y、Z在周期表中位置关系如图:
|
|
|
X |
|
|
Y |
|
|
Z |
|
|
(1)x元素的单质固态时是 ▲ 晶体。
(2)Y的气态氢化物的电子式为 ▲ ,固态时是 ▲ 晶体。。
(3)Z最高价氧化物的浓溶液和铜反应的化学方程式为 ▲
17.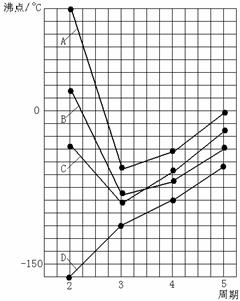 (8分)右图中A、B、C、D四条曲线分别表示IVA、VA、VIA、VIIA族元素的气态氢化物的沸点,其中表示VIA族元素气态氢化物沸点的是曲线 ▲ ;表示IVA族元素气态氢化物沸点的是曲线 ▲ ;同一族中第3、4、5周期元素的气态氢化物沸点依次升高,其原因是 ▲ ;A、B、C曲线中第2周期元素的气态氢化物的沸点显著高于第3周期元素气态氢化物的沸点其原因是 ▲
(8分)右图中A、B、C、D四条曲线分别表示IVA、VA、VIA、VIIA族元素的气态氢化物的沸点,其中表示VIA族元素气态氢化物沸点的是曲线 ▲ ;表示IVA族元素气态氢化物沸点的是曲线 ▲ ;同一族中第3、4、5周期元素的气态氢化物沸点依次升高,其原因是 ▲ ;A、B、C曲线中第2周期元素的气态氢化物的沸点显著高于第3周期元素气态氢化物的沸点其原因是 ▲
16.1,5-戊二醛(简称GA),是一种重要的饱和直链二元醛。2%的GA溶液具有广谱、高效、无刺激、无腐蚀等特点,对禽流感、口蹄疫、猪瘟等疾病有良好的防治作用。根据上述信息,判断下列说法中正确的是
A.戊二醛分子式为C5H10O2,符合此分子式的二元醛有4种
B.戊二醛不能在加热条件下和新制备的氢氧化铜反应
C.戊二醛不能使酸性KMnO4溶液褪色
D.2%的GA溶液能破坏菌体蛋白质,杀死微生物,具有消毒杀菌作用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com