
12.pH=2的两种一元酸HA和HB分别与足量锌粉反应,所生成的H2体积V(HA)>V(HB)。
下列说法正确的是 ( )
A.酸的物质的量浓度c(HA)一定大于c(HB)
B.HB一定不是弱酸
C.若两种酸体积相同,则HB的酸性比HA酸性强
D.这两种酸的物质的量浓度一定相同而体积不同
11.在一定温度下,NO2(g)转化为N2O4(g)是一个放热反应。在一个密闭容器中达到平衡后,改变下列条件,下列说法中错误的是 ( )
A.加压使体积变小,将使正、逆反应速率均增大,平衡时颜色加深
B.保持体积不变,加入少量NO2(g),将使逆反应速率减小
C.保持体积不变,升高温度,再达到平衡时混合物的颜色加深
D.保持体积不变,加入少量N2O4(g),再达到平衡时NO2(g)的体积分数变小
10.八角茴香含有一种抗H5N1型禽流感病毒的重要成分--莽草酸,其分子结构如图。下列关于莽草酸的说法错误的是 ( )
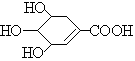 A.莽草酸分子式为C7H10O5
A.莽草酸分子式为C7H10O5
B.莽草酸能使溴水褪色
C.莽草酸遇FeCl3溶液不发生显色反应
D.1mol莽草酸可以与4molNaOH反应
9.通常条件下,下列各组物质不能用一种试剂通过化学反应区别的是 ( )
A.AgNO3 NaNO3 Na2CO3 B.Na2CO3 NaHCO3 K2CO3
C.MnO2 FeO CuO D.(NH4)2SO4 Na2SO4 NH4C1
8.下列说法或表示方法正确的是 ( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(石墨)→C(金刚石);△H= +1.91 kJ/mol,可知金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)==H2O(1);△H= -57.3 kJ/mol,若将含0.5 molH2SO4的浓硫酸与含l mol NaOH的稀溶液混合,放出的热量大于57.3 kJ
D.在101 kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)==2H2O(1);△H= +285.8 kJ/mol
7. 测得某无色透明溶液的pH=1,则在该溶液中一定能大量存在的离子组是 ( )
A.K+、Mg2+、Cl-、HCO3- B.Mg2+、Al3+、SO42-、NO3-
C.Na+、CH3COO-、NO3-、SO42- D.Na+、NH4+、Cl-、MnO4-
6.相同质量的CO2和N2O相比较,不一定相同的是 ( )
A.分子数 B.原子数 C.体积 D.电子数
25.如图,各物质有下转化关系:

请回答以下问题:
(1)若C是可用作自来水消毒的气体,D、E是含氧化合物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是 。
(2)若B、C均为常见非金属单质,D、E都是酸酐,则A是 ,D转化为E的化学反应方程式为 。
23.(1)某混合气体中可能含有N2、O2、Cl2、HCl、NH3、NO、NO2中的两种或多种气体,现将此无色透明的混合气体通过浓硫酸后,气体体积明显减小,当剩余气体与空气接触时,立即变为红棕色,则原混合气体中一定含有的气体是 ,一定不存的气体是 ,可能存在的气体是 。
(2)有下列物质:①溴化钾溶液 ②碘水 ③氯化亚铁溶液 ④二氧化碳;其中既能和硝酸银溶液反应,又能和氯水反应的是
(3)用排水集气法的50ml的试管中收集20ml NO后,仍倒立于水槽中,然后向试管内缓缓通入O2,试回答下列问题(气体体积在相同条件下测定)
a、试管中全部充满水时,应通入O2体积为
b、试管中的气体为原气体体积的1/2时,应通入O2体积为
c、试管中的气体体积不变时,应通入O2体积为
d、试管中全部充满气体时,应通入O2体积为
 24.电解原理在化学工业中有广泛应用。右图表示一个电解池,
24.电解原理在化学工业中有广泛应用。右图表示一个电解池,
装有电解液a:X、Y是两块电极板,通过导线与直流电源
相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始
时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是 。
②检验Y电极上电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是 ;X电极反应式是 。
22.称取吨铁粉11.20g,溶于过量的稀H2SO4中,加入5.05g KNO3晶体,并在加热条件下使溶液里的Fe2+部分氧化;再冷至室温,移入锥形瓶中,用0.50mol/L20mL的KMnO4溶液滴定达终点,已知有如下反应:
 KMnO4+FeSO4+H2SO4 Fe2(SO4)3+MnSO4+K2SO4+H2O
KMnO4+FeSO4+H2SO4 Fe2(SO4)3+MnSO4+K2SO4+H2O
(1)配平并完成KMnO4和FeSO4反应的化学方程式 。
(2)根据计算推断:a、酸性条件下,有 mol的Fe2+被KNO3氧化
b、硝酸钾与FeSO4反应的物质的量的比
c、KNO3与酸化的FeSO4溶液反应时,其还原产物是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com