
4.在一定条件下发生下列反应,其中属于盐类水解反应的是 ( )
A. HS-+H+=== H2S
B. NH4+ +2H2O 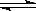 NH3·H2O + H3O+
NH3·H2O + H3O+
C.HCO3- + H2O
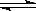 H3O+ + CO32- D.Cl2+H2O
H3O+ + CO32- D.Cl2+H2O 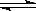 H++Cl-+HClO
H++Cl-+HClO
3.加热蒸干并灼烧(低于400℃)下列物质的溶液,可以得到该物质固体的是 ( )
A.氯化铝 B.碳酸氢钠 C.硫酸镁 D.高锰酸钾
2.在二氧化碳的饱和溶液中,C(H+)和C(CO32-)的比值 ( )
A.等于1 B.等于2 C.大于2 D.1-2之间
1.对于在一密闭容器中进行的反应:C(s)+O2(g)===CO2(g),下列说法中错误的是 ( )
A.将木炭粉碎成粉末状可以加快化学反应速率
B.升高温度可以加快化学反应速率
C.增加压强可以加快化学反应速率
D.增加木炭的量可以加快化学反应速率
25.(8分)在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如下(气体体积均为标准状况下测得):
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量/mg |
255 |
385 |
459 |
|
气体体积/mL |
280 |
336 |
336 |
(1)乙组实验中,盐酸 (填“过量”、“适量”或“不足量”),
理由是 。
(2)要计算盐酸的物质的量浓度,题中可做计算依据的是 。
(3)合金中Mg、Al的物质的量之比为 。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,能使合金中的铝恰好溶解,不形成铝的沉淀,并使Mg2+刚好沉淀完全,求所加NaOH溶液的体积。(写出计算过程)
24.(8分)已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH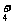 、Ba2+、Na+、H+、SO
、Ba2+、Na+、H+、SO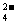 、NO
、NO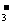 、OH-、CO
、OH-、CO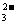 。将这四种溶液分别标记为A、B、C、D,进行如下实验:
。将这四种溶液分别标记为A、B、C、D,进行如下实验:
①在A或D中滴入C,均有沉淀生成
②D和B反应生成的气体能被A吸收
③A和D反应生成的气体能被B吸收
试回答下列问题:
(1)D的化学式是 ,判断理由是
。
(2)写出其余几种物质的化学式:A ;B ;C
(3)写出实验②中有关反应的离子方程式
。
23.(5分)向含有AlCl3和MgCl2的混合溶液中加入KOH溶液,若AlCl3与MgCl2物质的量之比为1:1。
(1) 请写出有关反应的化学方程式:
________________________________________________ ___________________
____________________________________ _______________________________
____________________________________ _______________________________
(2) 请画出析出沉淀的质量(纵坐标表示)与加入KOH溶液的体积 (横坐标表示)的示意图:
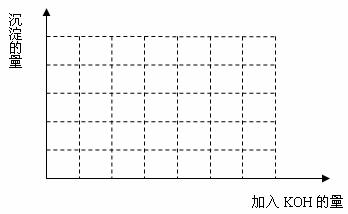
22.(8分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。请回答:
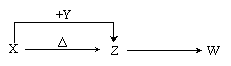
(1)W的电子式是 。
(2)X与Y在溶液中反应的离子方程式是 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体。

①装置Ⅰ中反应的化学方程式是 。
装置Ⅱ中物质的化学式是 。
②用Ⅹ含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 (从上图选择必要的装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,
该反应的化学方程式是 。
21.(9分)中学化学中几种常见物质的转化关系如下:
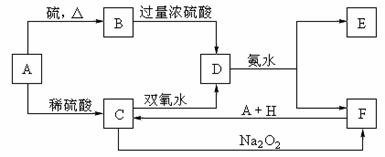
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体F粒子直径大小的范围: 。
(2)A、B、H的化学式:A ,B ,H 。
(3)①H2O2分子的电子式:
②写出C的酸性溶液与双氧水反应的离子方程式: 。
(4)写出鉴定E中阳离子的实验方法和现象:
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式: 。
20.(6分)(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
_____ _____+ ______ ____→
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com