
25£®(8·Ö)
ÒÑÖªÔÚ0.1mol¡¤L-1µÄNaHSO3ÈÜÒºÖÐÓйØ΢Á£Å¨¶ÈÓÉ´óµ½Ð¡µÄ˳ÐòΪ£ºc(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3)¡£Ôò£º
(1)Ôò¸ÃÈÜÒºÖÐc(H+)¡¡¡¡¡¡ c(OH-)(Ìî¡°<¡±¡°>¡±¡°=¡±)£¬¼òÊöÀíÓÉ(ÓÃÀë×Ó·½³ÌʽºÍ±ØÒªµÄÎÄ×Ö˵Ã÷)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)ÏÖÏòNH4HSO3ÈÜÒºÖУ¬ÖðµÎ¼ÓÈëÉÙÁ¿º¬ÓзÓ̪µÄÇâÑõ»¯ÄÆÈÜÒº£¬¿É¹Û²ìµ½µÄÏÖÏóÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»Ð´³ö¸Ã·´Ó¦µÄÀë×Ó·½³Ìʽ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
24£®(14·Ö)
ÅðËᾧÌå³ÊƬ״£¬Óл¬Äå¸Ð£¬¿É×÷È󻬼Á£¬ÅðËá¶ÔÈËÌåµÄÊÜÉË×éÖ¯ÓлººÍºÍ·À¸¯×÷Ó㬹ʿÉÒÔÓÃÓÚÒ½Ò©ºÍʳƷ·À¸¯µÈ·½Ãæ¡£ÊԻشðÏÂÁÐÎÊÌ⣺
(1)´ÓÌâÄ¿ÐÅÏ¢¿ÉÖªÅðËáÓ¦ÊôÓÚ¡¡¡¡¡¡ Ëá(Èõ¡¢Ç¿¡¢ÖÐÇ¿)
(2)ÅðËáµÄ·Ö×ÓʽΪH3BO3£¬ÒÑÖªHÓëO³É¼ü£¬ÔòÆä·Ö×ӽṹʽΪ£º¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(3)Ñо¿±íÃ÷£ºÔÚ´ó¶àÊýÇé¿öÏ£¬ÔªËصÄÔ×ÓÔÚÐγɷÖ×Ó»òÀë×Óʱ£¬Æä×îÍâ²ã¾ßÓдﵽ8µç×ÓÎȶ¨½á¹¹µÄÇ÷Ïò¡£ÒÑÖª0.01molÅðËá¿ÉÒÔ±»20mL 0.5mol¡¤L -1NaOHÈÜҺǡºÃÍêÈ«ÖкÍ,¾Ý´ËÍƲâÅðËáÔÚË®ÈÜÒºÖгÊËáÐÔµÄÔÒòÊÇ(ÓÃÀë×Ó·½³Ìʽ±íʾ)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ д³öÅðËáÓëNaOHÈÜÒº·´Ó¦µÄ»¯Ñ§·½³Ìʽ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
(4)ÅðËáºÍ¼×´¼ÔÚŨÁòËá´æÔÚµÄÌõ¼þÏ£¬¿ÉÉú³É»Ó·¢ÐÔÅðËáõ¥£¬ÊÔд³öÅðËáÍêÈ«õ¥»¯µÄ·½³Ìʽ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡
(5)¿Æѧ¼Ò·¢ÏÖÅð»¯Ã¾ÔÚ39 Kʱ³Ê³¬µ¼ÐÔ£¬ÔÚÅð»¯Ã¾¾§ÌåµÄÀíÏëÄ£ÐÍÖУ¬Ã¾Ô×ÓºÍÅð Ô×ÓÊÇ·Ö²ãÅŲ¼µÄ£¬Ò»²ãþһ²ãÅðÏà¼äÅÅÁУ¬ÓÒͼÊǸþ§Ìå΢¹Û¿Õ¼äÖÐÈ¡³öµÄ²¿·ÖÔ×ÓÑØZÖá·½ÏòµÄͶӰ£¬°×ÇòÊÇþÔ×ÓͶӰ£¬ºÚÇòÊÇÅðÔ×ÓͶӰ£¬Í¼ÖеÄÅðÔ×ÓºÍþÔ×ÓͶӰÔÚͬһƽÃæÉÏ¡£¸ù¾ÝÓÒͼȷ¶¨Åð»¯Ã¾µÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
Ô×ÓÊÇ·Ö²ãÅŲ¼µÄ£¬Ò»²ãþһ²ãÅðÏà¼äÅÅÁУ¬ÓÒͼÊǸþ§Ìå΢¹Û¿Õ¼äÖÐÈ¡³öµÄ²¿·ÖÔ×ÓÑØZÖá·½ÏòµÄͶӰ£¬°×ÇòÊÇþÔ×ÓͶӰ£¬ºÚÇòÊÇÅðÔ×ÓͶӰ£¬Í¼ÖеÄÅðÔ×ÓºÍþÔ×ÓͶӰÔÚͬһƽÃæÉÏ¡£¸ù¾ÝÓÒͼȷ¶¨Åð»¯Ã¾µÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
(6)ÅðÍé(B2H6)ÆøÌåÔÚ¿ÕÆøÖÐÄܾçÁÒȼÉÕÉú³É¹Ì̬Ñõ»¯ÎÒÑ֪ÿÉú³É1molҺ̬ˮ¿É·Å³ö722kJµÄÈÈÁ¿£¬ÇëдÈÈ»¯Ñ§·½³Ìʽ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
23£®( 9·Ö)
(1)Ç뽫5ÖÖÎïÖÊ£ºN2O¡¢FeSO4¡¢Fe(NO3)3¡¢HNO3ºÍFe2(SO4)3·Ö±ðÌîÈëÏÂÃæ¶ÔÓ¦µÄºáÏßÉÏ£¬×é³ÉÒ»¸öδÅäƽµÄ»¯Ñ§·½³Ìʽ¡£
_________+__________¡ú__________+__________+__________+H2O
(2)·´Ó¦ÎïÖз¢ÉúÑõ»¯·´Ó¦µÄÎïÖÊ__________£¬±»»¹ÔµÄÔªËØÊÇ_________¡£
(3)·´Ó¦ÖÐ1 molÑõ»¯¼Á_______(Ìî¡°µÃµ½¡±»ò¡°Ê§È¥¡±)___________ molµç×Ó¡£
(4)Ç뽫·´Ó¦ÎïµÄ»¯Ñ§Ê½¼°ÅäƽºóµÄϵÊýÌîÈëÏÂÁÐÏàÓ¦µÄλÖÃÖУº
¡¡ ¡¡ ¡¡¡¡¡¡¡¡ __________+¡¡¡¡¡¡¡¡ __________¡ú
22£®(13·Ö)
ÔÚ×ãÁ¿µÄÏ¡ÂÈ»¯ÑÇÌúÈÜÒºÖУ¬¼ÓÈë1-2µÎÒºä壬Õñµ´ºóÈÜÒº±äΪ»ÆÉ«¡£
(1)¼×ͬѧÈÏΪÕâ²»ÊÇ·¢Éú»¯Ñ§·´Ó¦ËùÖ£¬Ê¹ÈÜÒº±ä»ÆÉ«µÄÎïÖÊÊÇ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ (ÌîÁ£×ӵĻ¯Ñ§Ê½£¬ÏÂͬ)£»ÒÒͬѧÈÏΪÕâÊÇ·¢Éú»¯Ñ§·´Ó¦ËùÖ£¬Ê¹ÈÜÒº±ä»ÆÉ«µÄÎïÊÇ¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
(2)ÏÖÌṩÒÔÏÂÊÔ¼Á£º
A£®ËáÐÔ¸ßÃÌËá¼ØÈÜÒº¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®ÇâÑõ»¯ÄÆÈÜÒº
C£®ËÄÂÈ»¯Ì¼¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®ÁòÇ軯¼ØÈÜÒº
ÇëÅжÏÄÄλͬѧµÄÍƶÏÊÇÕýÈ·µÄ£¬²¢ÓÃÁ½ÖÖ·½·¨¼ÓÒÔÑéÖ¤£¬Ð´³öÑ¡ÓõÄÊÔ¼Á±àºÅ¼°ÊµÑéÖй۲쵽µÄÏÖÏó¡£
|
¡¡¡¡¡¡
ͬѧÕýÈ· |
Ñ¡ÓÃÊÔ¼Á |
ʵÑéÏÖÏó |
|
µÚÒ»ÖÖ·½·¨ |
¡¡ |
¡¡ |
|
µÚ¶þÖÖ·½·¨ |
¡¡ |
¡¡ |
(3)¸ù¾ÝÉÏÊöʵÑéÍƲ⣬ÈôÔÚÏ¡ä廯ÑÇÌúÈÜÒºÖÐͨÈëÂÈÆø£¬Ê×Ïȱ»Ñõ»¯µÄÀë×ÓÊÇ ¡¡¡¡
¡¡¡¡¡¡¡¡¡¡ £¬ÈôÑ¡Óõí·Ûµâ»¯¼ØÈÜÒºÀ´ÅжÏÄÄλͬѧµÄÍƶÏÊÇÕýÈ·µÄ£¬
ÄãÈÏΪÊÇ·ñ¿ÉÐÐ? ¡¡¡¡¡¡¡¡¡¡¡¡¡¡(Ìî¿ÉÐлò²»¿ÉÐÐ)
ÀíÓÉÊÇ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
21£®(6·Ö)
ÏÂÁÐÓйØʵÑéµÄÐðÊö£¬ÕýÈ·µÄÊÇ(ÌîÐòºÅ)(ÉÙÒ»¸ö¿ÛÒ»·Ö£¬¶àÒ»¸öµ¹¿ÛÒ»·Ö£¬¿ÛÍêΪֹ)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡£
¡¡ (A)ÅäÖÆ500mLijÎïÖʵÄÁ¿Å¨¶ÈµÄÈÜÒº£¬¿ÉÓÃÁ½Ö»250mLµÄÈÝÁ¿Æ¿
¡¡ (B)ÓÃÉøÎö·¨·ÖÀëµí·ÛÖлìÓеÄNaClÔÓÖÊ
¡¡ ¡¡(C)ÎÞ·¨Ó÷ÖҺ©¶·½«¸ÊÓͺÍË®µÄ»ìºÏÒºÌå·ÖÀë
¡¡ (D)ÓÃËáʽµÎ¶¨¹ÜÁ¿È¡20.00mL¸ßÃÌËá¼ØÈÜÒº
(E)ΪÁ˲ⶨijÈÜÒºµÄpH£¬½«¾Ë®ÈóʪµÄpHÊÔÖ½½þÈëµ½´ý²âÈÜÒº£¬¹ýÒ»»áÈ¡³ö£¬Óë±ê×¼±ÈÉ«¿¨½øÐжԱÈ
(F)ÓÃŨ°±Ë®Ï´µÓ×ö¹ýÒø¾µ·´Ó¦µÄÊÔ¹Ü
(G)ÅäÖÆÒø°±ÈÜҺʱ£¬½«Ï¡°±Ë®ÂýÂýµÎ¼Óµ½ÏõËáÒøÈÜÒºÖУ¬²úÉú³Áµíºó¼ÌÐøµÎ¼Óµ½³Áµí¸ÕºÃÈܽâΪֹ
(H) ÅäÖÆÒ»¶¨Å¨¶ÈµÄÈÜҺʱ£¬Èô¶¨ÈÝʱ²»Ð¡ÐļÓË®³¬¹ýÈÝÁ¿Æ¿µÄ¿Ì¶ÈÏߣ¬Ó¦Á¢¼´ÓõιÜÎüÈ¥¶àÓàµÄ²¿·Ö¡£
¡¡ (J)ÔÚÇâÑõ»¯Ìú½ºÌåÖмÓÉÙÁ¿ÁòËá»á²úÉú³Áµí
¡¡ (K)Óýᾧ·¨¿ÉÒÔ³ýÈ¥ÏõËá¼ØÖлìÓеÄÉÙÁ¿ÂÈ»¯ÄÆ
20£®»¯ºÏÎïA¡¢B¡¢C¡¢D¸÷ÓÉÁ½ÖÖÔªËØ×é³É£¬¼×¡¢ÒÒ¡¢±ûÊÇÈýÖÖµ¥ÖÊ¡£ÕâЩ³£¼ûµÄ»¯ºÏÎïÓëµ¥ÖÊÖ®¼ä´æÔÚÈçϹØϵ(ÒÑÖª»¯ºÏÎïCÊÇÒ»ÖÖÓлúÎï)£¬
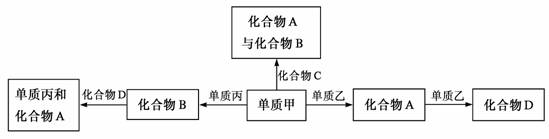
ÒÔϽáÂÛ²»ÕýÈ·µÄÊÇ
A£®ÉÏͼËùʾµÄÎå¸öת»¯¹ØϵÖУ¬ÓÐÈý¸öÊÇ»¯ºÏ·´Ó¦
¡¡¡¡ B£®ÉÏÊöת»¯¹ØϵËùÉæ¼°µÄ»¯ºÏÎïÖÐÓÐÒ»ÖÖÊǵç½âÖÊ
¡¡¡¡ C£®¼×¡¢ÒÒ¡¢±ûÈýÖÖµ¥Öʵľ§Ìå¾ùÊÇ·Ö×Ó¾§Ìå
D£®ÉÏͼËùʾµÄÎå¸öת»¯¹ØϵÖУ¬¾ùΪ·ÅÈÈ·´Ó¦
19£®ÎªÈ·¶¨Ä³ÈÜÒºµÄÀë×Ó×é³É£¬½øÐÐÈçÏÂʵÑ飺
¢Ù²â¶¨ÈÜÒºµÄpH£¬ÈÜÒºÏÔÇ¿¼îÐÔ¡£
¢ÚÈ¡ÉÙÁ¿ÈÜÒº¼ÓÈëÏ¡ÑÎËáÖÁÈÜÒº³ÊËáÐÔ£¬²úÉúÎ޴̼¤ÐÔ¡¢ÄÜʹ³ÎÇåʯ»ÒË®±ä»ë×ǵÄÆøÌå¡£
¢ÛÔÚÉÏÊöÈÜÒºÖÐÔٵμÓBa(NO3)2ÈÜÒº£¬²úÉú°×É«³Áµí¡£
¢ÜÈ¡ÉϲãÇåÒº¼ÌÐøµÎ¼ÓBa(NO3)2ÈÜÒºÖÁÎÞ³Áµíʱ£¬ÔٵμÓAg NO3ÈÜÒº£¬²úÉú°×É«³Áµí¡£
¸ù¾ÝʵÑéÒÔÏÂÍƲâÕýÈ·µÄÊÇ
A£®Ò»¶¨ÓÐSO32£Àë×Ó¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®Ò»¶¨ÓÐCO32£Àë×Ó
C£®²»ÄÜÈ·¶¨C1-Àë×ÓÊÇ·ñ´æÔÚ¡¡¡¡¡¡¡¡ D£®²»ÄÜÈ·¶¨HCO3£Àë×ÓÊÇ·ñ´æÔÚ
18£®Ä³Ñо¿ÐÔѧϰС×éΪÁË̽Ë÷þ·ÛÓëäåË®·´Ó¦µÄ»úÀí£¬×öÁËÈçÏÂËÄ×éʵÑ飺
¢Ù½«Ã¾·ÛͶÈëÀäË®ÖУ¬Î´¼ûÈκÎÏÖÏó£»
¢Ú½«Ã¾·Û·ÅÈëäåË®ÖУ¬¹Û²ìµ½Ö»ÊÇ¿ªÊ¼Ê±²úÉú¼«ÉÙÁ¿µÄÆøÅÝ£¬µ«äåË®µÄÑÕÉ«Öð½¥ÍÊÈ¥£»
¢Û½«Ã¾·Û·ÅÈëÒºäåÖУ¬Î´¹Û²ìµ½ÈκÎÃ÷ÏÔÏÖÏó£»
¢ÜÏòº¬×ãÁ¿Ã¾·ÛµÄÒºäåÖеμӼ¸µÎË®£¬¹Û²ìµ½äåµÄºì×ØÉ«ºÜ¿ìÍÊÈ¥¡£
ÔòÏÂÁйØÓÚþÓëäåË®µÄ·´Ó¦»úÀíµÄÂÛÊöÖÐÕýÈ·µÄÊÇ
A£®Ã¾·ÛÖ»Ö±½ÓÓëäåË®ÖеÄäå·´Ó¦
B£®Ã¾·ÛÖ»ÓëäåË®ÖеÄËá·´Ó¦
C£®²úÉú¼«ÉÙÁ¿µÄÆøÅÝÊÇÓÉÓÚþ·ÛÓëË®·´Ó¦µÃµ½
D£®Ã¾·ÛÔÚË®µÄ´ß»¯ÏÂÓëäå·¢Éú·´Ó¦
17£®¹ØÓÚÈçͼËùʾװÖõÄÐðÊö£¬ÕýÈ·µÄÊÇ
A£®ÍÊÇÑô¼«£¬ÍƬÉÏÓÐÆøÅݲúÉú¡¡¡¡¡¡¡¡¡¡ B£®ÍƬÖÊÁ¿Öð½¥¼õÉÙ
C£®µçÁ÷´ÓпƬ¾µ¼ÏßÁ÷ÏòÍƬ¡¡¡¡¡¡¡¡¡¡¡¡ D£®ÇâÀë×ÓÔÚÍƬ±íÃæ±»»¹Ô
16£®ÏÂÁз´Ó¦ÖУ¬Ñõ»¯¼ÁÓ뻹ԼÁÎïÖʵÄÁ¿µÄ¹ØϵΪ1¡Ã2µÄÊÇ
A£®O3+2KI+H2O==2KOH+I2+O2
 B£®2CH3COOH+Ca(ClO)2==2HClO+Ca(CH3COO)2
B£®2CH3COOH+Ca(ClO)2==2HClO+Ca(CH3COO)2
C£®I2+2NaClO3==2NaIO3+Cl2
D£®4HCl+MnO2==MnCl2+Cl2¡ü+2H2O
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com