
6、原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法不正确的是
A、由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+
B、由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O
C、由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
D、由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+
5、下列工业生产的说法错误的是
A、氯碱工业中隔离两电极的材料是阳离子交换膜,因此该生产工艺又称“阳离子交换膜法”
B、石膏可作为生产硫酸的原料之一
C、由于常压下SO2转化为SO3的转化率很高,所以SO2接触氧化时不采用高压的反应条件
D、合成氨的反应是放热反应,因此工业上合成氨常采用低温条件
4、下列实验操作能达到测量要求的是
A、用托盘天平称量25.20g氯化钠 B、用10mL量筒量取7.50mL稀硫酸
C、用25mL滴定管量取14.80mL溶液 D、用广泛pH试纸测得溶液的pH为4.2
3、时下,一种被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸酯产生能量,该能量被传递给荧光物质后便发生荧光。下列有关叙述中不正确的是
A、草酸酯中混有的草酸可用饱和碳酸钠溶液除去
B、草酸能使蓝墨水褪色
C、草酸受热时分解出来的气体产物是混合物
D、“魔棒”不能接近石油气之类的可燃性气体,否则可能会导致爆炸
1、近代10大科技突破中“火星上‘找’到水的影子”名列第一。下列说法中错误的是
A、用离子交换法可以使海水淡化
B、使用高效催化剂可使水分解,同时释放能量
C、4℃时水的密度最大,对水生动植物的生命活动有重大意义
D、水是金属发生电化学腐蚀的主要因素之一
|
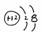 A、镁离子结构示意图
B、羟基电子式 H
A、镁离子结构示意图
B、羟基电子式 H

|
|
C、次氯酸电子式H D、氨分子结构
24. (10分)有如下化学反应:2A(g)+B(g)
2C(g)(△H<0=
(10分)有如下化学反应:2A(g)+B(g)
2C(g)(△H<0=
(1)若将4mol气体A和2mol气体B在2L密闭容器中混合,经2s后测得C的浓度为0.6mol·L-1。则2秒时B的浓度为 mol·L-1。
(2)若把amol气体A和b mol气体B充入上述密闭容器,达到平衡时,它们的物质的量满足n(A)+n(B)=n(C),则气体A的转化率为 。
(3)如下图所示,将4mol气体A和2mol气体B混合后置于体积可变的等压容器中,一定温度下达到平衡状态X时,测得气体总物质的量为4.2mol。若A、B、C起始的物质的量分别用a、b、c表示,试回答:

ⅰ:达到平衡状态X时的容器中,通入少量B气体,容器中A的体积分数 (填“增大”、“减小”或“不变”)。若要使A的体积分数再升高到与平衡状态X相同,可采取的一种措施是 (只填一种即可)。
ⅱ:若起始a=1.2mol,b=0.6mol,且达到平衡后各气体的体积分数与平衡状态X相同,则起始时C的取值范围为 。
23. (10分)已知:Ⅰ.CH3COONa+NaOH
CH4↑+Na2CO3
(10分)已知:Ⅰ.CH3COONa+NaOH
CH4↑+Na2CO3
|
 Ⅱ.R-CH==CH2+H2O
RCH2CH2OH
Ⅱ.R-CH==CH2+H2O
RCH2CH2OH
现有分子式C8H9Br的有机物在一定条件下能发生下图所示的一系列反应:
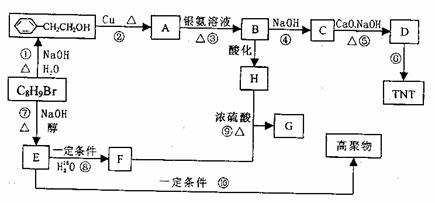
请回答下列问题:
(1)写出C8H9Br的结构简式: 。
(2)上述反应中属于消去反应的有(填编号) 反应。
(3)写出反应⑥、⑨的化学方程式:
反应⑥:
反应⑨:
(4)写出H可能有的3种同分异构体(要求:a.苯环上只有一个取代基,b.3种异构体不同类别):
22.(16分)某无色溶液中可能存在的离子如下: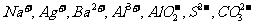
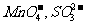 。取10mL该溶液进行实验,有关实验过程、现象及产物如下图所示:
。取10mL该溶液进行实验,有关实验过程、现象及产物如下图所示:

回答下列问题:
(1)沉淀D是(填名称) ,生成该沉淀的离子方程式为:
;
生成气体乙的离子方程式为: ;
生成沉淀F的离子方程式为: ;
(2)若测知气体甲为两种成分,则气体和原溶液中溶质的可能组成为(将结果填入下表中。)
|
可能情况 |
(1) |
(2) |
|
气体可能 组成 |
|
|
|
溶质可能组成 (填化学式) |
|
|
(3)若测知气体甲的成分只有一种时,则原溶液中一定存在的离子有 ,可能存在的离子有 。
|
21.(12分)某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了下图所示装置。打开分液漏斗D中活塞,缓慢加入稀盐酸至过量,与固体M充分反应。待反应停止后,B中有黑色沉淀析出,C中量气装置右边液面上升,调节量气装置使左右液面相平后,测得进入C中的气体为V mL(已换算成标准状况)。

根据上述实验事实,回答下列问题:
(1)加入药品和实验开始前必须进行的操作是 。
(2)固体M中一定有的物质是 (写化学式)。
(3)写出A中发生反应的化学方程式(只写一个):
。
(4)写出B中析出黑色沉淀时发生反应的离子方程式 。
(5)根据题给条件,固体M中一种物质的质量可以确定,应为 g(用代数式表示)。
(6)稀盐酸与固体M反应后还残留淡黄色固体,该固体可能是 (写化学式),要分离该固体,在实验操作中,除烧杯、玻璃棒外,还需要的玻璃仪器是 。
(7)反应完成后,取A中溶液少许加入试管中,要确定固体M中是否含有Fe3+,需加入的试剂为: 。
A.KSCN溶液 B.NaOH溶液 C.氨水
20.(14分)简要回答下列问题:
(1)春夏季下雨时常伴有“电闪雷鸣”现象,因“闪电”而发生的化学反应有(举两例,用化学方程式表示):
①
②
(2)酸雨的pH小于5.6,放置一段时间后pH还会减少。其原因是(用化学方程式表示):
(3)铁的纯度越高越不易生锈;钢铁表面上若附着有电解质更易生锈。铁锈的化学成分是:Fe2O3·nH2O。请写出钢铁生锈时有关反应的化学方程式(包括电极反应及其总反应):
电极反应式:
总反应式:
其它反应:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com