
13. 在一个固定体积为1L的密闭容器中,加入2 molA和1 molB发生如下反应:
2A(g)+B(g)
 3C(g)十D(s),达到平衡时C的浓度为1.2 mol/L。若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是
3C(g)十D(s),达到平衡时C的浓度为1.2 mol/L。若维持容器体积和温度不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是
A.4 mol A十2 mol B B.3 mol C+1 mol D+l mol B
C.3 mol C十0.7 mol D D.1.6 mol A+0.8 mol B+0.6 mol C+0.3 mol D
12.将Cu片放入0.1mol/L FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)为2:3,则Cu2+与Fe3+的物质的量之比为
A.3:2 B.3:5 C.4:3 D.3:4
11.下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是
|
|
(I) |
(II) |
|
A |
少量SO2通入Ba(OH)2溶液 |
过量SO2通入少量Ba(OH)2溶液 |
|
B |
少量浓氨水滴入Al2(SO4)3溶液 |
少量Al2(SO4)3溶液滴入浓氨水 |
|
C |
0.1mol
Cl2通入含0.2mol FeBr2的溶液 |
0.3
molCl2通入0.2molFeBr2溶液中 |
|
D |
过量BaCl2溶液与少量Na2SO4溶液相混合 |
少量Ba(NO3)2溶液与过量MgSO4溶液相混合 |
10. 在101KPa和25℃时,有反应的热化学方程式:
H2(g) + 1/2 O2(g) = H2O(g) △H=﹣241.8KJ/mol ;
H2(g) + 1/2 O2(g) = H2O(l) △H=﹣285.8KJ/mol 下列说法错误的是
A.H2燃烧生成H2O(g)时,放出241.8KJ的热量 B.H2的燃烧热为285.8KJ
C.O2前面的1/2表示参加反应的O2的物质的量
D.1mol液态水变成水蒸气时吸收44KJ的热量
9.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中共存的是
A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I-
B.pH为1的溶液:Cu2+、Na+、Mg2+、NO3-
C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+
D.所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+
8.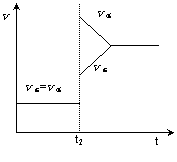 向某容积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)
向某容积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g) 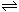 2HI(g),△H<0,当达到平衡后,t2时改变反应的某一条件(混合气体总物质的量不变),造成容器内压强增大,则下列说法中正确的是
2HI(g),△H<0,当达到平衡后,t2时改变反应的某一条件(混合气体总物质的量不变),造成容器内压强增大,则下列说法中正确的是
A.容器内气体的颜色变深,混合气体的密度增大
B.平衡不发生移动
C.转化率增大,HI平衡浓度变小
D.改变条件前后,速率图像如右图
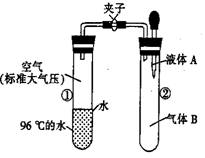
7. 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合一定不可能是下列的
A、氢氧化钠溶液.二氧化碳 B、水.氨气
C、氢氧化钠溶液.一氧化氮 D、水.二氧化氮
6.钡和钠相似,也能形成O22-离子的过氧化物,则下列叙述错误的是
A.过氧化钡的化学式是Ba2O2
 B.1mol过氧化钠或过氧化钡跟足量水反应都生成0.5mol氧气
B.1mol过氧化钠或过氧化钡跟足量水反应都生成0.5mol氧气
C.过氧化钡是离子化合物
D.过氧化钠和过氧化钡都是强氧化剂
5.用NA表示阿伏加德罗常数,下列说法正确的是:
①18g D2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4LSO3的物质的量为1mol ⑤4℃时5.4mL的水所含的原子总数为0.9NA ⑥0.1molOH-含0.1NA个电子 ⑦1mol Na2O2与水完全反应时转移电子数为2NA
A.③⑤⑥⑦ B.③⑤ C.①②④⑦ D.③④⑤⑥
4.近期报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80Mpa下合成出金刚石,具有深远意义。下列说法不正确的是
A.由二氧化碳合成金刚石是化学变化 B.金刚石是碳的一种同位素
C.钠在空气中最终能生成碳酸钠 D.金刚石中只含有非极性共价键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com