
23. (8分) 甲、乙、丙、戊都具有如下图所示的结构或结构单元,图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同。已知:甲、乙是同一类晶体,晶体中有各自的结构单元,单质甲能与乙发生置换反应。丙、丁、戊三种粒子含有等量的电子数,其中丙、丁是同一类晶体中的分子或分子集团,常温下丁呈液态,能产生两种等电子数的粒子,戊是阳离子。
(8分) 甲、乙、丙、戊都具有如下图所示的结构或结构单元,图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同。已知:甲、乙是同一类晶体,晶体中有各自的结构单元,单质甲能与乙发生置换反应。丙、丁、戊三种粒子含有等量的电子数,其中丙、丁是同一类晶体中的分子或分子集团,常温下丁呈液态,能产生两种等电子数的粒子,戊是阳离子。
(1) 写出液态丁产生两种等电子粒子的
电离方程式: 。
(2) 室温下含有戊的盐溶液,其pH 。
A.>7 B.=7 C.<7 D.以上都有可能
(3) 丙是目前重要的能源。
丙和丁在催化、加热条件下得到可燃性的两种气体,其反应的化学方程式是
。
(4) 甲、乙高温反应时,若乙平均被破坏了4 mol共价键,则参加反应的乙为 g。
22.(10分)对溶液中的反应,下列图象中n表示生成沉淀的物质的量,m表示沉淀的质量,v表示参加反应的一种反应物的物质的量,根据相关图象回答问题:
[可选择的物质:CO2、NaOH、Ba(OH)2、KA1(SO4)2 ]
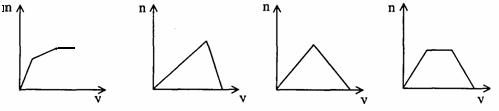
A B C D
(1)反应过程产生沉淀量符合A图像的两种反应物为 。
(2)反应过程产生沉淀量符合B图像的离子反应式为 。
(3)反应过程产生沉淀量符合C图像的离子反应式为 。
(4)反应过程产生沉淀量符合D图像的反应物为 。
21.(12分)A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,B、C、D属同一周期,A、E在周期表中处于同一纵行.已知:①除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子;②A与B,B与D都能生成非极性分子,B与C生成的气态非极性分子为直线型分子;③D与E生成离子化合物,其离子的电子层结构相同.回答:
(1)A为________元素(填名称,下同),B为________元素,C为________元素,
D为________元素,E为________元素;
(2)C元素在周期表中属第________周期,________族元素;
(3)D与B形成的化合物的电子式__ __,属________晶体;
(4)C与E形成的化合物的电子式为____________和____________,属______晶体.
20.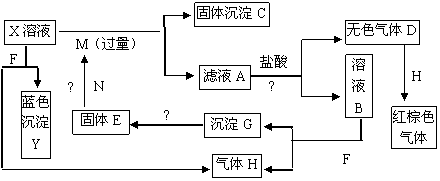 (10分)如下图,已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的最高价氧化物是耐火材料,它的晶体硬度很大,常做手表的轴承;H为单质。下图中部分反应产物已略去。
(10分)如下图,已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的最高价氧化物是耐火材料,它的晶体硬度很大,常做手表的轴承;H为单质。下图中部分反应产物已略去。
⑴红棕色气体及X的化学式分别为 、 。
⑵反应①的离子方程式为_______________________________________________。
反应②的化学方程式为_______________________________________________。
19.(10分)海水的综合利用可以制备金属镁,其流程如下图所示:
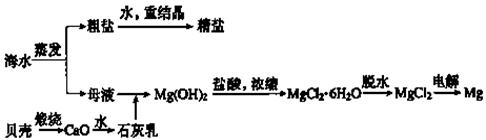
(1) 若在空气中加热MgCl2·6H2O生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式_________________________________________________________________;
(2)Mg(OH)2沉淀中混有Ca(OH)2应怎样除去?写出实验步骤。
____________________________________________________________________________;
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发步骤的操作中都要用到玻璃棒,下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是(填字母代号)_______ 。
A.一定溶质质量分数溶液的配制
B.用适量的蔗糖、浓硫酸和水在小烧怀中进行浓硫酸的脱水性实验
C.用普通漏斗组成的过滤装置进行过滤实验
D.用浓氨水和浓盐酸进行氨和氯化氢反应的实验
E.用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验
F.硫酸铜晶体里结晶水含量测定的实验
G.将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体
18. (14分) 有20.6gNH4HCO3和NaHSO3的干燥粉末状混合物,用加热分解的实验方法,通过测定生成的二氧化碳质量来测定NH4HCO3的质量分数。根据下图所示的仪器和所盛试剂填空。
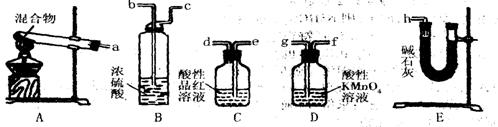
(1)按气流由左向右的方向连接仪器的顺序(用a---h表示)为
(2)仪器B的作用为 ;E装置中放碱石灰的仪器的名称为 ;
A和E装置中都用到的仪器名称为 。
(3)D的作用是 。
(4)C的作用是 ;若C瓶中溶液颜色有变化,则测定结果将会偏
(5)若碱石灰的质量增加8.8g,则混合物中NH4HCO3的质量分数为 。
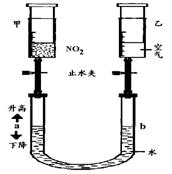
17.(8分)在常温、常压下,注射器甲中装有NO2气体,
注射器乙中装有同体积的空气(如图所示,夹持仪器均已略去)。
(1)常温下,打开两个止水夹后,同时向外拉动两注射器
的活塞,且拉动的距离相同,将会看到U型管中
液面a (升高、下降、不变),
试解释这一现象 。
(2)如将注射器甲中的气体换成NH3,仍在常温下,打开两个止水夹后,同时向里
推动两注射器的活塞,且推动的距离相同,将会看到U型管中液面a (升高、下降、不变),试解释这一现象 ____________________。
16.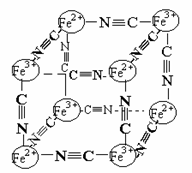 分析化学中常用X射线研究晶体结构.有一种蓝色晶体{可表示为:MxFey(CN)Z
},研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的点, 自身互不相邻,而CN-位于立方体的棱上.其晶体中的部分离子的空间结构关系如图示,下列说法正确的是
分析化学中常用X射线研究晶体结构.有一种蓝色晶体{可表示为:MxFey(CN)Z
},研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的点, 自身互不相邻,而CN-位于立方体的棱上.其晶体中的部分离子的空间结构关系如图示,下列说法正确的是
A.该晶体属于原子晶体
B.该晶体化学式MFe2(CN)6
C.M的离子位于上述立方体的体心,呈+1价
D.该晶体属于离子晶体,M呈+2价
 第Ⅱ卷(非选择题 共86分)
第Ⅱ卷(非选择题 共86分)
15.A、B、C、D、E是同周期的五种元素。已知A和B的最高价氧化物对应的水化物呈碱性,且碱性B>A;C和D的气态氢化物的水溶液呈酸性,且酸性C>D;五种元素的简单离子中,E的离子半径最小,则它们的原子序数由大到小的顺序是
A、C、D、E、A、B B、E、C、D、A、B
C、B、A、E、D、C D、B、A、D、C、E
14.下列反应的离子方程式错误的是
A.等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B.氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O
C.足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32-+H2O=2NaHCO3↓
D.向碳酸氢钠溶液中滴入过量澄清石灰水:
Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com