
28.(15分)下面是关于药物华素片(西地碘片)使用说明中的部分内容:
|
华素片(西地碘片)使用说明书 [品名和组成] 品名:西地碘片 商品名:华素片 英文名:Gydiodine tablets 华素片(西地碘片)的主要活性成分是分子碘,含量1.5mg/片。 将碘利用分子分散技术制成分子态西地碘,并含适量薄荷脑等。 [贮藏]遮光、密闭、在阴凉处保存 [有效期]二年 |
(1)根据上述说明和所学化学知识回答: ①华素片中含有的活性成分是________(写分子式);
②请推断华素片__________(“是”或“不是”)白色的。
(2)某学生为验证华素片中确实含有上述成分,完成实验如下。请填空:
①取一粒药片放入研钵中研碎,再将药粉装入试管并加入约2mL蒸馏水;向试管中加入约0.5mL________(填选项字母),并用力振荡。
A.酒精 B.热裂汽油 C.四氯化碳 D.甘油
②描述加入该液体后可能观察到的现象___________________________。
(3)请再设计另一种方法,验证华素片中的成分(注意叙述实验操作方法和实验结论)。
____________________________________________________________________
____________________________________________________________________。
27.(15分)不同元素的原子在分子内吸引电子的能力大小可用数值x来表示。若x越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷的一方。下面是某些短周期元素的x值:
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x值 |
0.98 |
1.57 |
2.04 |
2.55 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
(1)通过分析x值变化规律,确定N、Mg最接近的x值范围:
_______<x(Mg)______,______<x(N)<______。
(2)推测x值与原子半径关系是___________ _______。上表中短周期元素x值的变化特点,体现了元素性质的______ _____变化规律。
(3)某有机化合物结构式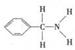 ,其中C-N键中,你认为共用电子对偏向于________(写原子名称)一方。
,其中C-N键中,你认为共用电子对偏向于________(写原子名称)一方。
(4)经验规律告诉我们:当成键的两原子相应元素的x差值(Δx)即Δx>1.7时,一般为离子键;Δx<1.7时,一般为共价键。试推断:AlBr3中化学键类型是___ ______。
(5)预测x值最小的元素在周期表中的具体位置______ __(放射性元素除外)
13.将3.20gCu跟30.0mL10.0mol·L-1的HNO3充分反应,还原产物有NO和NO2,若反应后溶液中有a molH+,则被还原的HNO3物质的量是
A.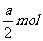 B.
B.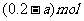 C.
C.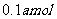 D.
D.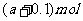
第Ⅱ卷 (非选择题 共10题 共174分)
|
|
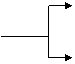
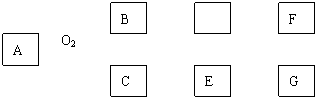 26.(15分)物质的转化关系如下图所示,其中甲可由两种单质直接化合得到,乙为金属单质,它在G的浓溶液中发生钝化,F的溶液中只含一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)
26.(15分)物质的转化关系如下图所示,其中甲可由两种单质直接化合得到,乙为金属单质,它在G的浓溶液中发生钝化,F的溶液中只含一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)


|
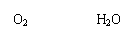


 请分别对以下两种情况填空:
请分别对以下两种情况填空:
(1)若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近时,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。则:
①1.7gA与O2反应生成气态的B和C时放出22.67kJ热量,写出该反应的热化学方程式:_______。
②D与乙反应的离子方程式是__________________________。
(2)若B为红棕色固体,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成。则:
①工业上反应Ⅰ在__ ___(填设备名称,下同)中进行。反应Ⅱ在__ ____中进行。
②甲的化学式为____ ____。
③D和乙反应的离子方程式是_______________________________。
12.设NA表示阿伏加德罗常数的值,下列说法中正确的是
A.将分子总数为NA的NH3和HCl两种气体混合置于标准状况下,其体积约为22.4L
B.14g氮气中所含的共用电子对数为1.5NA
C.1L1mol·L-1FeCl3溶液中,含自由移动的Fe3+的个数为NA
D.合成氨反应中,当断裂3NA人H-H共价健的同时生成6NA个N-H共价键,则该反应
达到平衡
11.pH相同的氨水、NaOH和Ba(OH)2三种溶液,分别用蒸馏水稀释到原体积的x倍、y倍和z倍。稀释后三种溶液的pH仍然相同,则x、y、z的关系是
A.x>y=z B.x=y=z C.x>y>z D.x>z>y
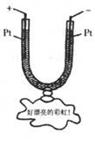
10.如图所示,在U形管中装入滴有紫色石蕊试液且混合均匀的某溶液,通直流电,一段时间后U形管内会形成一个倒立的“彩虹”,则U形管内的溶液可能为
A.H2SO4溶液 B.NaOH溶液 C.AgNO3溶液 D.Na2SO4溶液
9.在短周期中的X和Y两种元素可组成化合物XY3,则下列说法正确的是
 A.若X的原子序数是m,则Y的原子序数必定是m+4
A.若X的原子序数是m,则Y的原子序数必定是m+4
B.XY3晶体一定属于离x子晶体
C.X与Y可属于两个不同周期,也可属于同一周期
D.X的原子半径小于Y的原子半径
8.某溶液既能溶解SiO2,又能完全溶解乙酸乙酯,在该溶液中可以大量共存的离子组是
A.K+、Na+、HCO3-、Cl- B.Ag+、NH4+、SO42-、Br-
C.Mg2+、H+、NO3-、SO42- D.K+、Na+、AlO2-、CO32-
7.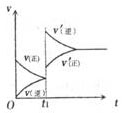 对达到平衡状态的可逆反应:A+B
对达到平衡状态的可逆反应:A+B C+D,在t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D的状态叙述正确的是
C+D,在t1时增大压强,正、逆反应速率变化如图所示,下列有关A、B、C、D的状态叙述正确的是
A.A、B、C为气体,D不是气体
B.A、B为气体,C、D有一种为气体
C.C、D为气体,A、B有一种为气体
D.C、D有一种为气体,A、B都不是气体
6.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性。制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子的直径在5.5nm-36nm的滋流体。下列说法中正确的是
A.所得的分散系属于悬浊液 B.该分散系能产生丁达尔效应
C.所得的分散系中分散质为Fe2O3 D.给分散系通直流电时,阳极周围黑色加深
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com