
19.(14分)(1)常温下,将一定量CO2通入NaOH溶液中,二者恰好完全反应,得到只含一种溶质A的溶液A的溶液,且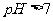 ,向该溶液中加入BaCl2溶液,生成白色沉定B。B不可用作钡餐,若误用了B,可用5%的钠盐溶液C处理。请回答:
,向该溶液中加入BaCl2溶液,生成白色沉定B。B不可用作钡餐,若误用了B,可用5%的钠盐溶液C处理。请回答:
①用离子方程式表示A溶液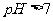 的原因
。
的原因
。
②用离子方程式表示B不可用作钡餐的原因 。
③用离子方程式表示出误用B后可用C处理的原因 。
 (2)在2L的密闭容器中,把3molA和4molB混合,在一定温度下发生反应:
(2)在2L的密闭容器中,把3molA和4molB混合,在一定温度下发生反应:

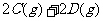
该反应2min后达到化学平衡,生成2molC,A的体积分数为w%。
回答下列问题:
①2min内A的化学反应速率为 。
②此条件下该反应的化学平衡常为 ,B的转变率为 。
③若在相同条件下向该容器中充入amolA、bmolB、cmolC、dmolD,某时刻达到平衡,A的体积分数仍为w%,则a与c满足的关系为 。
18.(8分)A、B、C、D四种短周期元素,原子序数依次递增,A原子形成的阳离子就是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数B原子的核外电子总数相等,D在同周期元素中原子半径最大。A、C、D三种元素可形成化合物甲,甲为中学化学常见物质。请回答:
(1)甲中所含化学键的类型为 。
(2)已知乙是A、B两元素形成的最简单的有机化合物,依据乙在氧气中完全燃烧的反应设计成燃料电池,若以氢氧化钾溶液做电解质溶液,写出该电、池的负极反应式
。
(3)由A、B、C三种元素组成的化合物B2A4C在一定条件下可以转化为B2A4C,写出实现该转化的化学方程式 ,B2A4C在一定条件下转化为B2A4C2。B2A6C2在一定条件下能发生反应,写出该反应的化学方程式 。
17.(12分)苛研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为: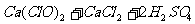 △
△ 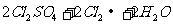
他们设计如下制取氯气并验证其性质的实验。
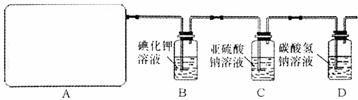
请回答:
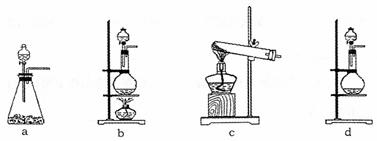
(1)该实验中A部分的装置是 (填写装置的序号)。
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):
(3)写出在D装置中发生反应的离子方程式
。
(4)该实验存在明显的缺陷,请你提出改进的方法。
(5)该小组又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1mol·L-1的Na2S2O3溶液做标准液滴定反应生成的碘,已知反应式为;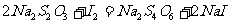 ,共用去Na2S2O3溶液20.0 mL。则该漂白粉中
,共用去Na2S2O3溶液20.0 mL。则该漂白粉中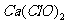 的质量分数
。
的质量分数
。
16.(4分)下列叙述不正确的是 (填字母)。
A.用滴有酚肽的水做氨的喷泉实验,只验证了氨的溶解性
B.容量瓶上有温度、容积和刻度线
C.在两支试管中分别加热氯化铵和碳酸氢铵,现象完全相同
D.在试管中分别加入3mL乙醇,然后边摇动试管边加入2mL浓流酸和2mL乙酸,加入2-3块碎瓷片,用酒精灯小心加热可制取乙酸乙酯
E.在两支试管中分别加入少量乙酸乙酯,然后向第一支试管中加入稀硫酸,向第二支试管中加入NaOH溶液,直接用酒精灯加热,可比较两者水解的程度
F.在铝热反应的实验中,用滤纸做漏斗必须干燥
15.向含有1molKAl(SO4)2的溶液中逐滴加入Ba(OH)2溶液,充分反应,下列说法不正确的是 ( )
A.当A13+恰好完全沉淀时,消耗Ba(OH)21.5mol
B.当SO42-恰好完全沉淀时,A13+全部转化为[A1(OH)4]
C.当向溶液中加入1.5molBa(OH)2时,反应可用下列离子方程式表示:
 2A13++3SO2-4+3Ba2++6OH- 2A1(OH)3↓+3BaSO4↓
2A13++3SO2-4+3Ba2++6OH- 2A1(OH)3↓+3BaSO4↓
D.随加入的Ba(OH)2的物质的量不断增大,沉淀物质的量不断增大
第Ⅱ卷 综合题(共70分)
14.下列实验过程中产生的现象与对应的图形相符合的是 ( )
 A.NaHSO3粉末加入HNO3溶液中 B.SO2气体通入新制氯水中
A.NaHSO3粉末加入HNO3溶液中 B.SO2气体通入新制氯水中
C.NaOH溶液滴入Ba(HCO3)2溶液中 D.CO2气体通入澄清石灰水中

13.已知亚硝酸(HNO2)是一种弱酸,其酸性略强于醋酸。亚硝酸钠能与氢碘酸(HI)发生反应成一氧化氧和碘单质。下列说法不正确的是 ( )
A.亚硝酸钠与氢碘酸反应的离子方程式是2H++NO2-+2I-=I2+NO↑+H2O
B.相同温度下,同浓度的醋酸钠溶液的pH大于亚硝酸钠溶液的pH
C.氮氧化物与雨水反应生成硝酸和亚硝酸,是酸雨的成分
D.用淀粉碘化钾试纸、食醋、冷开水可以区别食盐和亚硝酸钠
12.下列化学方程式或离子方程式正确的是 ( )
A.碳酸氢钠与溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
B.单质铜与稀硝酸反应:Cu+2H++2NO3-=Cu2++2NO↑+H2O
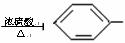
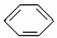
C.苯与硝酸反应 +HO-NO2 NO2+H2O
D.铝片跟氢氧化钠溶液反应:A1+2OH-+2H2O=[A1(OH)4]-+H2↑
11.已知0.1mol·L-1的二元酸H2A溶液的pH=4,则下列是说法中正确的是 ( )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有c(Na+)> c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有c(Na+)>c(A2-)>c(H+)>c(OH-)
10. 在一定条件下,对于可逆反应X(g)=+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol·L-1、0.3mol·L-1、0.8mol·L-1,则下列判断不合理的是 ( )
在一定条件下,对于可逆反应X(g)=+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol·L-1、0.3mol·L-1、0.8mol·L-1,则下列判断不合理的是 ( )
A.c1:c2=1:3 B.平衡时,Y和Z的生成速率之比为2:3
C.X、Y的转化率相等 D.c1的取值范围为0< c1<0.14mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com