
8.分子式为C5H7Cl的有机物,其结构不可能是 ( )
A.只含有一个双键的直链有机物 B.含有两个双键的直链有机物
C.含一个双键的环状有机物 D.含一个叁键的直链有机物
7.常温时,下列四种液体pH最小的是 ( )
A.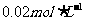 的醋酸与
的醋酸与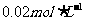 的NaOH溶液等体积的混合液
的NaOH溶液等体积的混合液
B.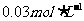 的醋酸与
的醋酸与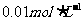 的NaOH溶液等体积的混合液
的NaOH溶液等体积的混合液
C.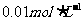 的醋酸溶液
的醋酸溶液
D.pH=2的盐酸与pH=12的NaOH溶液等体积的混合液
6.某温度下,100g饱和氯化钠溶液中含有氯化钠26.5g。若向此溶液中添加3.5g固体氯化钠和6.5g水,则所得溶液的溶质质量分数是 ( )
A.30% B.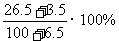
C.26.5% D.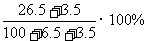
5.下列叙述错误的是 ( )
A.第ⅦA族的砹化银见光容易分解,难溶于水
B.第ⅥA族的H2O、H2S、H2Se随着相对分子质量的增大,沸点逐渐升高
C.第ⅣA族的H2CO3比H2SiO3酸性强,故将CO2通入Na2SiO3溶液中有H2SiO3析出
D.第ⅢA族的氢氧化铊[Tl(OH)3]不一定呈两性
4.NA表示阿伏加德罗常数的值,下列叙述中正确的是 ( )
A.1L 1mol·L-1醋酸溶液中离子总数为2NA
B.标准状况下,22.4LH2中含中子数为2NA
C.46gNO2和N2O4混合气体中含有的原子数为3NA
D.1mol-OH中所含电子数为10NA
3.下列离子在溶液中可以大量共存,且向溶液中加入铝粉能产生氢气的是 ( )
A.K+、Cl-、Na+、SO B.Na+、OH-、Cl-、Ba2+
B.Na+、OH-、Cl-、Ba2+
C.H+、Cl-、Fe2+、NO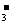 D.Cu2+、OH-、CO
D.Cu2+、OH-、CO 、Na+
、Na+
2.下列说法中正确的是 ( )
①元素的相对原子质量是该元素原子的质量与一个12C原子质量的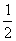 的比值
的比值
②质子数相同的微粒一定属于同一种元素
③分子是保持物质性质的一种微粒
④原子是物质变化中的最小微粒
⑤同一种元素组成的单质是纯净物
A.均不正确 B.②⑤正确 C.③④正确 D.①②正确
1.下列叙述正确的是 ( )
①工业上合成非氧 化物陶瓷氮化硅(Si3N4)需要在高温、空气气氛中进行
②钢铁制品锈蚀主要是因为钢铁中含有碳而发生原电池反应,因此生铁炼钢时要尽可能完全除去生铁中的碳
③建设三峡大坝需要使大量水泥,水泥是硅酸盐材料
④夏天人们佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
⑤太阳能电池可采用硅材料制作,其应用利于环保、节能
A.①②③ B.②④ C.③④⑤ D.③⑤
21.(13分)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘版上的铜箔,制造印刷电路板。某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
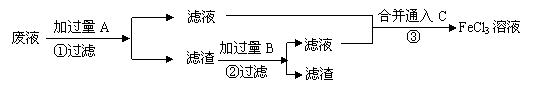
(1)写出一个证明还原性Fe比Cu强的离子方程式 ,该反应在上图步骤 中发生。请根据上
述反应设计一个原电池,在方框中画出简易装置图
(标出极名称、电极材料、电解质溶液)。
(2)分别写出上图步骤②、③相关反应的化学方程式:
步骤② 。
步骤③ 。
(3)上述过程回收的铜是粗铜,为了获得更纯的铜必须进行电解精炼。写出电解精炼时阳极材料及电极反应式 。
20.(9分)下图所示转化关系中涉及的物质均由短周期元素组成(部分产物已略去),其中M由X、Y两种同周期元素组成,X原子的最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数为6。请填写下列空白:
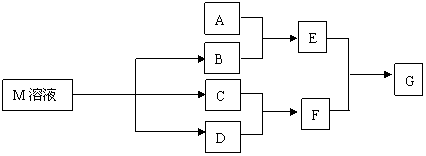
(1)若A是第3周期某一元素的氧化物,当F的水溶液过量时,G为可溶性盐,F的水溶液不足时,G为沉淀,则E与过量F反应的离子方程式为
。
(2)若A是一种常见酸性氧化物,且可用于制造玻璃,则A与B反应的化学方程式为
。
(3)若A是一种常见化肥,式量为79,且E与F反应生成G时,有白烟产生,则A与足量B加热时反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com