
18. (18分)某化学研究小组为证明CO具有还原性,首先查阅相关的资料,获取下列信息:
(18分)某化学研究小组为证明CO具有还原性,首先查阅相关的资料,获取下列信息:
|
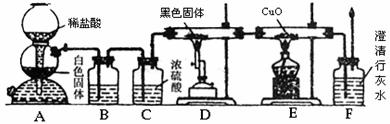
请回答下列问题:
(1)装置A中反应的离子方程是 。
(2)装置B最适宜的试剂是 ;必须用装置C吸收气体中水蒸气的理由是
。
(3)按照如图装置进行实验时,首先进行的操作是 ,并要排净整套装置中的空气,则排净装置中空气的必要性是
; 。
(4)根据该实验中的 现象,可证明CO具有还原性,有关反应的化学方程式是 。
(5)若要根据装置F中石灰水变浑浊的现象确认CO具有还原性,应在上图装置
与
之间连接下图中的
装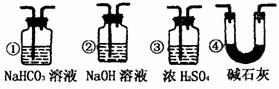 置(填序号)。
置(填序号)。
 19.(8分)830K时,在密闭容器中发生下列可逆反应CO+H2O(g) CO2+H2 △H<0。
19.(8分)830K时,在密闭容器中发生下列可逆反应CO+H2O(g) CO2+H2 △H<0。
试回答下列问题:
(1)若起始时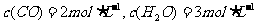 ,达到平衡时CO的转化率为60%则平衡常数K=
,此时水蒸气的转化率为
。
,达到平衡时CO的转化率为60%则平衡常数K=
,此时水蒸气的转化率为
。
(2)在相同温度下,若起始时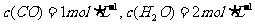 ,反应进行一段时间后,测得H2的浓度为
,反应进行一段时间后,测得H2的浓度为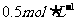 ,则此时该反应是否达到平衡状态 (填“是”与“否”),此时
,则此时该反应是否达到平衡状态 (填“是”与“否”),此时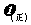
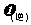 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)若降低温度,该反应的K值将 ,该反应的化学反应速率将 (均填“增大”“减小”或“不变”)。
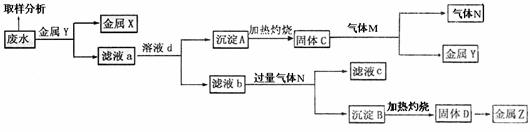
17.(8分)某工厂排出的废水中含有Ag+、Fe3+、Al3+三种金属离子。某同学设计了如下流程从废水中提取三种金属(流程中部分物质没有标出)。
 回答下列问题:
回答下列问题:
(1)固体C的化学式为 ,滤液b中通入过量气体N发生反应的离子方程式为
,固体D转化为金属Z的化学方程式为 。
(2)取样分析废水Ag+、Fe3+、Al3+的含量,目的是
a.控制溶液中Ag+、Fe3+、Al3+含量比
b.确定下一步加入金属Y的量
c.确定滤液a中加入溶液d的量
d.确定沉淀A转化为固体C所需的温度
16.(8分)下图表示物质X发生的变化,其中每一个方格代表一种反应物或生成物(部分生成物没有标出)。
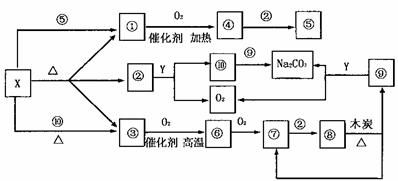
试填写下列空白:
(1)物质X可能为 或 :物质Y为 。
(2)写出③转化为⑥的化学方程式 。
15.一定温度下,mg下列物质在足量的氧气中充分燃烧后,产物与足量的Na2O2固体充分反应,固体质量增加了ng,且n>m符合要求的物质是 ( )
A.HCOOCH3 B.CH3CHO C.HOOC-COOH D.C6H12O6
第Ⅱ卷(非选择题,共55分)
14.某实验室仅有如下仪器或用具:烧杯、铁架台、铁圈、三角架、普通漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、滤纸、火柴。从缺乏仪器或用具的角度看,不能进行的实验操作项目是 ( )
A.过滤 B.蒸发 C.萃取 D.溶解
13.有机物 在不同条件下至少可能发生下列7种不同类型的有机
反应:①加成反应 ②取代反应 ③消去反应 ④氧化反应 ⑤酯化反应 ⑥加聚反应 ⑦缩聚反应。上述反应中可以体现醇羟基性质的有 ( )
A.①④⑥⑦ B.③④⑤ C.②③④⑤⑦ D.①②③④⑤
12.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10)如下图,则下列判断错误的是 ( )
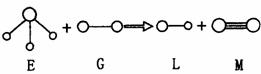
A.G是最活泼的非金属单质 B.L可用于刻蚀玻璃
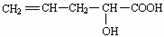 C.E能使紫色石蕊试液变蓝色 D.M的化学性质活泼
C.E能使紫色石蕊试液变蓝色 D.M的化学性质活泼
11.1mol下列固体物质①Na2O ②NaOH ③Na2O2 ④Na2SO3长期放置在空气中,固体质量增加的关系(不考虑潮解因素)正确的是 ( )
A.①=②>③>④ B.①>③>④>②
C.②>①=③>④ D.④>②>③>①
10.叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是 ( )
A.HN3水溶液中微粒浓度大小顺序: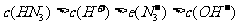
B.HN3与NH3作用生成的叠氮酸铵是共价化合物
C.NaN3水溶液中离子浓度大小顺序: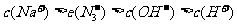
|
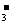 与CO2所含电子数相等
与CO2所含电子数相等9.对于某些离子的检验及结论一定正确的是 ( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO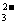
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH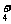
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com