
6.运用元素周期律分析下面的推断,其中推断错误的是 ( )
A.氢氧化铍(Be(OH)2)的碱性比氢氧化镁弱
B.哎(At)为有色固体;Hat不稳定;AgAt感光性很强,且不溶于水也不溶于稀酸
C.硫酸锶(HrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)是无色、有毒,比H2S稳定的气体
5.下列各组物质的分类都正确的是(括号里的是类别) ( )
A.空气(混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质)
B.液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质)
C.HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃)
D.NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯)
3.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子。N4分子结构如右图所示,下列说法正确的是 ( )
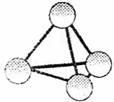 A.N4属于一种新型的化合物
A.N4属于一种新型的化合物
B.N4转化为N2属于物理变化
C.N4的摩尔质量为56
D.N4与N2互为同素异形体
|
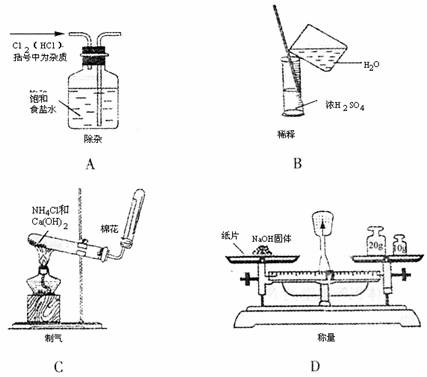
2.背景材料:①2006年5月信息时报报道:世界卫生组织建议每人每天钠的摄取量应少于2000毫克,长期过量摄入钠可能引起高血压、肾病、胃病;②2004年冬季,诺贝尔化学奖授予研究蛋白质的科学家;③2006年初夏,四川大部分地区进行人工降雨;④2005年春末,某高速公路发生液氯运输车翻倒泄露事故。下列相应说法不正确的是 ( )
A.钠单质是一种活泼金属,常常保存在煤油中
B.蛋白质是由氨基酸形成的不可降解的高分子化合物,其水溶液有丁达尔现象
C.AgI和干冰都可用于人工降雨
D.附近人员应迅速远离液氯泄露地点,并逆风往安全区域疏散
1.为了防止瓦斯爆炸,可采取的措施有:a、定期检查矿井内瓦斯的浓度,保持矿井内有良好的通风状况;b、定期向矿井内撒石灰粉,以除去矿井内的瓦斯;c、用矿井通风和控制瓦斯涌出的方法,防止瓦斯浓度超标;d、定期向矿井内喷洒水,以保持矿井内空气湿润;e、杜绝一切非生产需要的火源;f、矿工戴上防毒面具,以防不测。其中正确的是( )
A.abce B.ace C.acde D.acef
24.(11分)铜是重要的工业原材料,现有Cu、Cu2O和CuO组成的混合物,某研究性学习小组为了探究其组成情况,向混合物中加入100mL0.6moL/LHNO3溶液刚好使其溶解,同时收集到224mLNO气体(标准状况)。请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的化学方程式 ;
(2)产物中硝酸铜的物质的量 mol;
(3)如混合物中含0.01 molCu,则其中Cu2O、CuO的物质的量分别是 mol、 mol;
(4)如混合物中Cu的物质的量为X,则X的取值范围为 。
23.(7分)已知X是一种碱式盐,H是常见金属单质,F、I是常
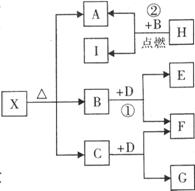 见非金属单质,E、G都是工业上重要的碱性物质,它们有右
见非金属单质,E、G都是工业上重要的碱性物质,它们有右
图所示的关系。
试回答下列问题:
(1)G的化学式为: 。
(2)写出下列反应的化学方程式
① ,
② 。
(3)X在医药上用作解酸剂,与盐酸作用时,生成B的物质
的量与消耗盐酸的物质的量之比为3:8,则X的化学
式为: 。
22.(7分)A、B、C、D均为短周期元素。A、B可形成两种液态化合物,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。已知X分子与B2A分子中的电子数相等。Y分子与最简式为BA的分子中的电子数相等。请回答:
(1)写出元素的名称:A ,C 。
(2)Y分子是 分子(填极性和非极性)。
(3)写出实现下列转化的化学反应方程式并标明电子转移的方向和数目:
C2+(BA)n→A2
(4)B4A3D2水溶液呈酸性,写出其呈酸性的离子方程式:
21.(8分)在完全满足可逆反应:2H2O(g)  2H2+O2,2CO+O2
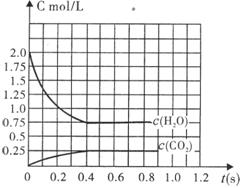
2H2+O2,2CO+O2 2CO2能顺利进行的条件下,将2molH2O(g)和2molCO充入l L密闭容器中,使其发生反应,一段时间后反应达到平衡。反应过程中部分气体浓度随时间t的变化情况如下图所示:
2CO2能顺利进行的条件下,将2molH2O(g)和2molCO充入l L密闭容器中,使其发生反应,一段时间后反应达到平衡。反应过程中部分气体浓度随时间t的变化情况如下图所示:
(1)请在图中画出c(H2)随时间t的变化曲线图;
 (2)平衡时c(O2)平为
mol/L。
(2)平衡时c(O2)平为
mol/L。
(3)欲计算出平衡时O2的浓度,除已知“H2O(g)
和CO”的物质的量外,至少需要知道平衡体
系中某两种气体的平衡浓度。这两种气体除
可以是H2O和CO2外还可以是 。
(4)在其它条件不变的情况下,若改为起始时在
容器中充入2molH2和2molCO2,则上述两反
应达到平衡时,c(O2)平= mol/L。
20.(6分)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。已知水是反应产物之一。
(1)该反应中还原剂是 ;
(2)该反应中还原产物是 ;
(3)若反应过程中转移了0.3mol电子,则生成水的质量是 g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com