
5.下列有关叙述正确的是 ( )
A.在中和滴定中,既可用标准溶液滴定待测溶液,也可用待测溶液滴定标准溶液
B.进行中和滴定操作时,眼睛要始终注视滴定管内溶液液面的变化
C.测定中和热时,两烧杯间填满碎纸的作用是固定小烧杯
D.若用50mL 0.55mol·L-1的氢氧化钠溶液,分别与50mL 0.50mol·L-1的盐酸和50mL 0.50mol·L-1硫酸反应充分反应,两反应的中和热不相等
4.对于化学反应能否自发进行,下列说法中错误的是 ( )
A.若△H<0,△S>0,任何温度下都能自发进行
B.若△H>0,△S<0,任何温度下都不能自发进行
C.若△H>0,△S>0,低温时可自发进行
D.若△H<0,△S<0,低温时可自发进行
3.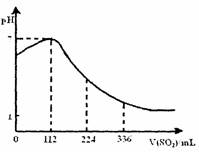 某同学向100mL氢硫酸溶液中通入标准状况下的
某同学向100mL氢硫酸溶液中通入标准状况下的
二氧化硫气体,所得溶液pH变化如图所示。他据
此得到的下列四条关于二氧化硫和亚硫酸的说法。
请分析其中正确的是 ( )
A.SO2是弱电解质
B.H2SO3不是强酸
C.亚硫酸是比氢硫酸还弱的酸
D.原氢硫酸溶液的物质的量浓度0.05mol·L-1
2.现用氯水来制取含有次氯酸的溶液,既要提高溶液中HClO物质的量浓度,又要降低溶液中HCl浓度,下列措施可以采用的是 ( )
A.加热挥发HCl B.加水使平衡向正反应方向移动
C.加NaOH中和HCl D.加CaCO3中和HCl
1.向水中加入下列物质,其中能使水的电离程度增大的物质是 ( )
A.NaCl B.NH4Cl C.HCl D.NaOH
29.(14分)某校课外活动小组为测定某碳酸钠、碳酸氢钠混合物样品中各组分的含量,设计了两组方案。
(1)第一组同学想通过图1所示仪器来达到实验目的。如想成功的话,还需要的仪器有
、 (填仪器名称)。

(II)第二组同学设计了图2装置。为达到实验目的,需在A、C两个虚框中各填入图3中E、F两个仪器中的一个(可重复使用)。请回答下列问题:
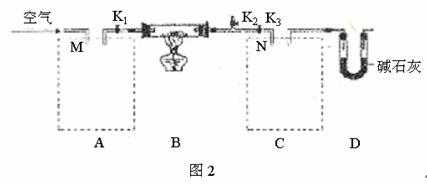

(1)已知样品质量为mg,C增重mg,A中M接 ,C中N接
(填接口序号),则NaHCO3的质量分数为 。
(2)若D装置不存在,将导致NaHCO3的质量分数 (填“偏大”、“偏小”或“不变”)。
(3)加热之前的操作中处于关闭状态的活塞是 ;加热过程中处于关闭状态的活塞是 。
28.(16分)有些化合的具有相同的相对分子质量,如本题涉及的A、E、L、M四种物质的相对分子质量均为58。其中A、F均为烃的含氧衍生物.A可由B催化氧得到,但A无法进一步被催化氧化;F能发生银镜反应;L是K的同系物,其碳原子不可能在同一平面上;M是一种无机弱碱,可被G所溶解。各物质之间的相互转化关系见下图;
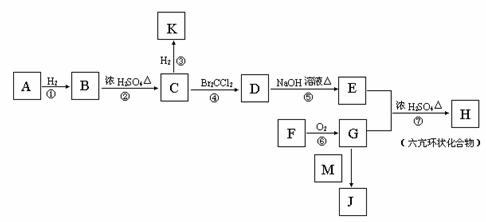
回答下列问题:
(1)写出下列反应的反应类型:反应② ,反应⑦ ;
(2)写出下列物质的结构简式:A ,F ,L ,
H ;
(3)写出下列反应的化学方程式:
D→E: ,
G+M→J: 。
27.(15分)现有A、B、C、D、E五种短周期元素,原子序数依次递增。其中A、E位于同一主族,B、C、D位于同一周期,A、E原子序数之和为B原子序数的2倍,B、D原子最外层电子数之和是C原子最外层电子数的2倍。它们中只有两种元素能形成固体单质。请回答下列问题:
(1)B元素的元素符号是 ;
(2)D、E两元素形成的原子个数比1:1的化合物的电子式为 ;
(3)0.1mol·L-1由A、D、E三元素形成的化合物的水溶液中,水电离产生的OH-液度c(OH-)水为 mol·L-1;
(4)过量Fe与C的最高价氧化物对应水化物稀溶液反应的离子方程式为
;
(5)由以上五种元素中的几种可以形成两种20电子化合物,向甲的溶液中加入乙可以影响甲的电离,甲的电离方程式为 ;
(6)在A、C、D形成的化合物中,C元素有两种价态,其绝对值之和为8,则其水溶液中各种离子浓度由大到小的顺序为 。
26.(15分)一定温度下,将A2和B2加入固定容积的2L密闭容器中,发生如下反应:
 A2(g)+3B2(g) 2AB3(g);
A2(g)+3B2(g) 2AB3(g);
(1)下列各项中,能表明该反应一定达到化学平衡状态的是 (填序号)
①正反应速率和逆反应速率相等
②容器内混合物的密度不再发生变化
③A3的质量不再发生变化
④单位时间内生成n molA3的同时生成了3n molB2
⑤容器内的总压强保持恒定
⑥A2、B2、AB3的物质的量之比为1:3:2
(2)若起始时加入1molA2和3molB2,半分钟时A2的物质的量浓度为0.2mol·L-1,则半分钟内B2的反应速率为 mol·L-1·s-1;若反应达平衡时混合物的总物质的量为2.5mol,则A2的转化率为 。
(3)若向(2)已在平衡的容器中再充入1molA2和3molB2,此时平衡将
(填“向左移动”或“向右移动”或“不移动”)。
13. ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。可通过以下反应制得ClO2;
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。可通过以下反应制得ClO2;
2KClO3+H2C2O3+H2SO4 2ClO2↑K3SO4+2CO3↑+2H2O,下列说法正确的是( )
A.KClO3在反应中失去电子 B.ClO2是氧化产物
C.H3C3O4在反应中被氧化 D.1molKClO3参加反应有2mol电子转移
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com