
22、(8分)有A、B、C、D四种短周期元素,A、B、C为同一周期依次相邻的3种元素,A和C的原子序数之比为3:4,且A、B、C分别与D形成三种化合物分子所含的电子数相等,请回答:
⑴X、Y、Z、W都是由上述元素中的两种组成的化合物,若X分子的空间构型为三角锥型,则X的电子式为 ;已知Y被称为绿色氧化剂,Z与Y具有相同的电子数,两者在液态时常一起作为火箭推进器的燃料,且已知0.8gZ与Y作为火箭推进剂时,能放出20.44KJ的能量(产物均为气态),请写出该反应的热化学方程式:
W是中学化学中常见的物质,其分子的空间构型为直线型,且所含有的原子数多于2个,其可能的化学式为 、 (只要写出2个)。
⑵甲、乙、丙都是由上述元素中的三种组成的物质,甲为食品中常见的天然高分子化合物,表示其组成的化学式为
;乙属于无机盐类,其水溶液明显显酸性,则乙的化学式为
;丙与甲的组成元素相同,丙的溶液呈弱酸性,其式量小于80,且其中A的质量分数为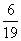 ,则丙的结构简式为
。
,则丙的结构简式为
。
21、 (10分)已知A、B、E是固体化合物,D、G是固体单质,X、Z、F为可燃性气体,F、X的火焰呈淡蓝色,他们之间有如下转化关系:
(10分)已知A、B、E是固体化合物,D、G是固体单质,X、Z、F为可燃性气体,F、X的火焰呈淡蓝色,他们之间有如下转化关系:
⑴写出A、B、Z的名称:A ,B ,Z
⑵写出Y的结构式: ,A的晶体结构类型: ,
溶液H的保存要求 ;
⑶按要求写出反应方程式:
①的化学方程式:
⑥离子方程式:
20、(14分)向溴水中加入足量的乙醛溶液,可以看到溴水褪色,对产生该现象的原因有如下三种猜想:①溴水与乙醛发生取代反应;②由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应;③由于乙醛具有还原性,溴水将乙醛氧化为乙酸。为探究哪种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中Br2的物质的量和反应后溶液中Br-离子的物质的量。
⑴方案一是否可行 填“是”或“否”),理由是 。
⑵假设测得反应前溴水中Br2的物质的量为amol,若测得反应后n(Br-)= mol,则说明溴水与乙醛发生取代反应;若测得反应后n(Br-)= mol,则说明溴水与乙醛发生加成反应;若测得反应后n(Br-)= mol,则说明溴水将乙醛氧化为乙酸。
⑶按物质的量之比为1:5配制1000mLKBrO3-KBr溶液,该溶液在酸性条件下完全反应可生成0.5molBr2。 取该溶液10mL加入足量乙醛溶液,使取褪色,然后将所得溶液稀释为100mL,准确量取其中10mL,加入过量的AgNO3溶液,过滤、洗涤、干燥后称量得到固体0.188g。若已知CH3COOAg易溶于水,试通过计算判断溴水与乙醛发生反应的类型为 (选填猜想序号)。
⑷写出上述测定过程中的三个反应的离子方程式:
①KBrO3和KBr在酸性条件下的反应 : ;
②溴水与乙醛的反应: ;
③测定Br-离子含量的反应: ;
19、(4分)下列有关化学实验的操作或说法中,正确的是(填写字母代号)
A、实验室制取肥皂时,将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂
B、进行中和热测定实验时,需要测出反应前盐酸与NaOH溶液的各自温度及反应后溶液的最高温度
C、检验红砖中的氧化铁成分时,向红砖粉末中加入盐酸,放置到充分沉淀后,取上层清液于试管中,滴加KSCN溶液2~3滴即可
D、制备硫酸亚铁晶体时,向稀硫酸中加入废铁屑至有少量气泡发生时,过滤,然后加热蒸发滤液即可得到硫酸亚铁晶体
E、进行纤维素水解实验时,把一小团脱脂棉放入试管中,滴入少量90%的浓硫酸搅拌,使脱脂棉变成糊状,再加入一定量的水,加热至溶液呈亮棕色,然后加入新制的
Cu (OH)2加热至沸腾即可
18、某些盐在溶液中结晶时,析出的晶体是结晶水合物。下表记录了t℃的4份相同的硫酸铜溶液中加入的无水硫酸铜的质量以及析出的硫酸铜晶体(CuSO4·5H2O)的质量(温度维持不变)的实验数据
|
硫酸铜 |
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
|
加入的无水硫酸铜(g) |
2.5 |
4.0 |
6.0 |
8.0 |
|
析出的硫酸铜晶体(g) |
0.10 |
2.8 |
6.4 |
10.0 |
当加入4.6g无水硫酸铜时,析出硫酸铜晶体的质量为
A、3.42g B、3.88g C、6.82g D、2.56g
第II卷(选择题 共78分)
17、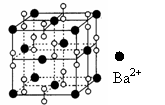 钡在氧气中燃烧时的得到一种钡的氧化物晶体,起结构如下图所示,有关说法正确的是
钡在氧气中燃烧时的得到一种钡的氧化物晶体,起结构如下图所示,有关说法正确的是
A、该晶体属于离子晶体
B、晶体的化学式为Ba2O2
C、该晶体晶胞结构与CsCl相似
D、与每个Ba2+距离相等且最近的Ba2+共有12个
16、下列离子方程式不正确的是
A、三氯化铝溶液中加入过量氨水:Al3++3OH―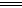 Al(OH)3↓
Al(OH)3↓
B、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:
4AlO2―+7H++H2O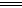 3Al(OH)3↓+Al3+
3Al(OH)3↓+Al3+
C、在Mn2+的溶液中加入HNO3再加入PbO2,得紫红色溶液:
5PbO2+2Mn2++4H+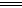 5Pb2++2MnO4-+2H2O
5Pb2++2MnO4-+2H2O
D、将0.1mol/L盐酸数滴缓缓滴入0.1mol/L25mLNa2CO3溶液中,并不断搅拌:
2H++CO32-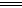 CO2↑+H2O
CO2↑+H2O
15、2005年诺贝尔化学奖被授予“在烯烃复分解反应研究方面作出贡献”的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如2分子烯烃RCH=CHR'用上述催化剂作用会生成两种新的烯烃RCH=CHR和R'CH=CHR'。则分子式为C4H8的烯烃中,任取两种发生“复分解反应”,生成新烯烃种类最多的一种组合中,其新烯烃的种类为
A、5种 B、4种 C、3 种 D、2种
14、对于平衡体系mA(g)+nB(g)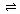 pC(g)+qD(g);△H<0。下列结论中正确的是
pC(g)+qD(g);△H<0。下列结论中正确的是
A、若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.48倍,
则m+n>p+q
B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n
C、若m+n=p+q,则往含有a mol气体的平衡体系中再加入b mol B,达到新平衡时,气体的总物质的量等于(a+b)
D、温度不变时,若压强增大至原来的2倍,达到新平衡时,总体积一定比原体积的1/2要小
13、含工业染色剂“苏丹红一号”的有毒食品曾流入市场,引起人们的恐慌。研究表明:核黄素(即维生素B2)能缓解“苏丹红一号”的毒性,其结构如下图
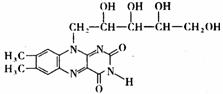 下列有关核黄素的说法中,正确的是
下列有关核黄素的说法中,正确的是
A、核黄素属于分子晶体
B、核黄素能发生银镜反应
C、核黄素属于糖类
D、核黄素不能被酸性高锰酸钾溶液氧化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com