
5.下列表述正确的是
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
②提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料
③化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
④太阳能电池可采用硅材料制作,其应用有利于环保、节能
⑤游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
A.①②③ B.③④⑤ C.②④ D.③⑤
4.分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④根据反应中的热效应将化学化学反应分为放热反应和吸热反应
A.①③ B.②④ C.①②④ D.②③④
3.设NA表示阿伏加德罗常数,下列叙述中,正确的是 ( )
A.常温常压下,16gO2和O3的混合物中共含有NA个氧原子
B.假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA
C.78gNa2O2固体中所含阴、阳离子总数为4NA
D.在铜与硫的反应中,1mol铜原子参加反应失去的电子数为2NA
2.实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是
A.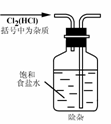 B.
B.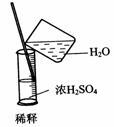
C.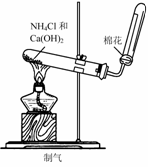 D.
D.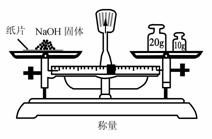
1.化学与科技、社会、生产密切结合,下列做法合理合法的是
A.汽油中添加乙醇制备“乙醇汽油”,可有效减少有害气体的排放。
B.养鸭厂添加苏丹红制“红心鸭蛋”,可使鸭蛋色泽鲜艳、美观。
C.化妆品中添加含铬物质制美白润肤“SK-Ⅲ”,可使女性青春永驻。
D.汽水中添加林丹、毒死蜱和七氯等杀虫剂制“可口可乐、百事可乐”,增强口感和余味。
26.(12分)在一定温度下将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应:3A(g)+B(g)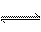 2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,请填写下面空白。
2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,请填写下面空白。
(1)B的平衡浓度为 。
(2)A的转化率为 。
(3)用D表示的平均反应速率为 。
(4)如果缩小容器容积(温度不变),则平衡体系中混合气体的密度、平均相对分子质量__________、__________。(两空均填“增大、“减少”或“不变” )
(5)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3 mol,要使平衡时各物质的质量分数与原平衡相等,则还应加入 mol B物质。
25、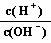 (4分)
(4分)
(1)常温下,将1mL pH = 1的H2SO4溶液加水稀释至100mL ,稀释后的溶液中 =
;
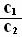 (2)常温下,pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5 的Al2(SO4)3溶液中由水电离出的H+ 浓度为c2,则 = ;
(2)常温下,pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5 的Al2(SO4)3溶液中由水电离出的H+ 浓度为c2,则 = ;
24.(12分)某校化学小组学生利用图12装置进行“氨的催化氧化及其产物验证”实验。(图中夹持装置已略去)
 (1)装置B中盛放的试剂是__________(填名称),用来吸收混合气体中的水汽。
(1)装置B中盛放的试剂是__________(填名称),用来吸收混合气体中的水汽。
(2)反应开始时,将装置C中铂丝加热到红热,撤去酒精灯,铂丝变暗。此时鼓入空气,铂丝又变红热。这是因为氨的催化氧化是_________反应。
(3)实验过程中,装置D中的导管容易生成无色晶体而堵塞。为了解决该问题,可以在活塞a后增加______(选填序号)。
①盛有蒸馏水的洗气瓶 ②盛有浓盐酸的洗气瓶 ③盛有碱石灰的U形管
(4)反应一段时间后,装置E中的气体颜色应为 色。此时,装置E中的含氮化合物有NH3、NO、NO2、___________(填化学式)。
(5)反应一段时间后,装置F中的紫色石蕊试液变红,其原因是(写出化学方程式)__________________________________________________。
(6)实验结束时,应__________________________,并停止鼓入空气。
(7)工业上合成氨的反应是:N2(g)+3H2(g)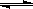 2NH3(g);△H= -92.2kJ·mol-1。
2NH3(g);△H= -92.2kJ·mol-1。
①下列做法能够提高工业合成氨转化率的是_________(选填字母)
a.增大压强 b.升高温度
c.使用铁触媒 d.将生成的NH3及时从混合气体中分离出去
②工业合成氨时采用500℃左右的温度,主要是因为:
____________________________________________________________ 。
23.(8分)如下图所示的装置,C、D、E、F、X、Y都是惰性电极。

将电源接通后,向乙中滴入酚酞液,在F极附近显红色。试回答以下问题:
(1)电源A极的名称是_______。
(2)甲装置中电解反应的总反应离子方程式是:____________________________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是______________。
(4)欲用丙装置给铜镀一层银,G应该是_______(填“铜”或“银”),电镀液的主要成分是________________(填化学式)。
(5)装置丁中的现象是_________________________________ _____,
说明___________________________________ 。
22.(12分)甲、乙、丙、丁、戊分别是Na2SO4、Ba(NO3)2、HNO3、BaCl2、NaOH五种溶液中的一种,现利用X溶液鉴别它们,已知气体B的密度在同温同压下是氢气密度的22倍。试根据下图中的转化关系回答问题:
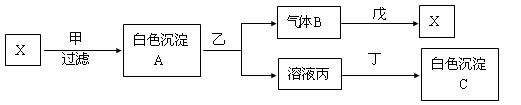
(1)下列物质的化学式分别为:
甲 、 乙 、丙 、丁 、X ;
(2)白色沉淀A与乙反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com