
28.(10分)
下图A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C 点显红色,请填空:
(1)电源A的a为 极。
(2)滤纸B上发生的总反应方程式为: 。
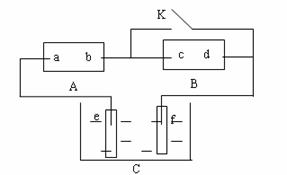
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为: ,电极f上发生的反应为: ,槽中盛放的镀液可以是 或 (只要求填两种电解质溶液)。
27.(12分)A、B、C、D、E、F、G、H八种短周期元素,其单质的沸点如下图所示。
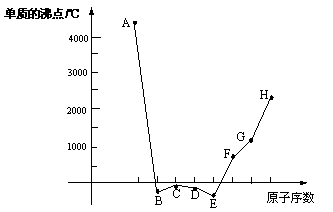
请回答:
(1)上述元素的最高价氧化物的水化物中,碱性最强的是(写电子式) ;上述元素的气态氢化物中,最稳定的是(写电子式) 。
(2)上述元素中,某些元素的常见单质所形成的晶体为分子晶体,这些单质的分子式是 。
(3)已知D、F、G三种元素的离子具有跟Ne相同的电子层结构,则这三种离子的半径由大到小的次序为(用相关元素的离子符号表示): > > 。
(4) 在101kPa时, B的氢化物1g 在C的单质中充分燃烧,生成一种液态化合物和另一种对环境无污染的稳定物质,放出18.6kJ的热量。该反应的热化学方程式为
26.(6分) 臭氧(O3)可以使湿润的淀粉碘化钾试纸变蓝。化学方程式为: KI + O3
+ H2O-- KOH + I2 + O2(配平)
(1)该反应中氧化剂为 ,还原产物为 ;
(2)若消耗0.1 mol氧化剂,反应中转移电子的物质的量为 ___ 。
25.根据表中的数据,下列说法错误的是
|
|
NaCl |
CnH2n+2 |
C4H10 |
CH4 |
SiCl4 |
单质B |
|
熔点(℃) |
810 |
-130 |
-138.4 |
-182 |
-68 |
2300 |
|
沸点(℃) |
1465 |
36.1 |
a |
-164 |
57 |
2500 |
A.SiCl4是分子晶体 B.单质B可能是原子晶体
C.n > 4 D.a < -164
第II 卷 (共50分)
24.下列事实与氢键有关的是
A.水加热到很高的温度都很难分解
B.水结成冰体积膨胀
C.CH4、SiH4、GeH4、SnH4熔点随相对分子量增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱
23.下列各分子中,所有原子都满足最外层为8电子结构的为:
A. HCOOH B.PCl5 C.P4 D.BF3
22. 下列各组热化学方程式程中,化学反应的△H前者大于后者的是
①C(s)+O2(g)=CO2(g);△H1 C(s)+1/2O2(g)=CO(g);△H2
②S(s)+O2(g)=SO2(g);△H3 S(g)+O2(g)=SO2(g);△H4
③H2(s)+1/2O2(g)=H2O(g);△H5 2H2(g)+O2(g)=2H2O(l);△H6
④CaCO3(s)=CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)=Ca(OH)2(s);△H8
A.① B.④ C.②③④ D.①②③
21.已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列结论正确的是
A.碳的燃烧热大于110.5kJ/mol
B.①的反应热为221kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
20.下列离子方程式中,正确的是
A.在氯化亚铁溶液中通入氯气 Fe2+ +Cl2 = Fe3+ +2Cl-
B.氯化铝溶液跟过量氨水反应 Al3+ +3NH3•H2O = Al(OH)3↓+3NH4+
C.碳酸氢钙溶液跟稀硝酸反应 Ca(HCO3)2 +2H+ = Ca2++2H2O+2CO2↑
D.铜片跟稀硝酸反应: Cu +2NO3-+4H+ = Cu2+ +2NO2+2H2O
19.据报道,某星球大气中含有一种称为硫化羰(COS)的化合物,其分子结构与CO2类似,能在O2里燃烧。下列说法正确的是
A.CO2是非极性分子而COS是极性分子 B.CO2与COS均无还原性
C.固体COS是原子晶体 D.COS是一种酸性氧化物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com