
15.下列离子方程式中正确的是
A.硫化亚铁放入盐酸中 S2-+2H+==H2S↑
B.硫酸铜溶液中通入硫化氢 Cu2++H2S==CuS↓+2H+
C.氯化铝溶液中加入过量氨水 Al3++4NH3·H2O==AlO2-+4NH4++2H2O
D.碳酸氢铵溶液中加入过量氢氧化钠溶液 HCO3-+OH-==CO32-+H2O
14.加热装有1 molHI气体的定容密闭容器,在t1 ℃,2HI(g)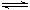 H2(g)+I2(g);△H>0反应达到平衡时,I2的物质的量分数为x1;若起始时在该容器中加入2 molHI,在t2 ℃达到平衡时,I2的物质的量分数为x2;则下列关系正确的是
H2(g)+I2(g);△H>0反应达到平衡时,I2的物质的量分数为x1;若起始时在该容器中加入2 molHI,在t2 ℃达到平衡时,I2的物质的量分数为x2;则下列关系正确的是
A.若t1=t2,则x1=x2 B.若t1=t2,则x1<x2
C.若t1<t2,则x1=x2 D.若t1<t2,则x1<x2
13.标准状况下,集满二氧化氮气体的烧瓶(容积为1 L)倒置于水槽中,液面上升到某一位置后不再变化,假设烧瓶内溶质不扩散,且忽略烧瓶内外液面差引起的压强差,则所得HNO3浓度(mol·L-1)及剩余气体体积的关系正确的是
A.=1/22.4 =1/3 B.<1/22.4 <1/3
C.>1/22.4 >1/3 D.<1/22.4 >1/3
12.室温下,向20 mL0.1 mol/L的盐酸溶液中逐滴加入0.1 mol/L的氨水至过量,在此过程中,溶液中各离子浓度关系一定错误的是
A.c(NH4+)>c(Cl-)>c(H+)>c(OH-) B.c(Cl-)=c(NH4+)>c(H+)=c(OH-) C.c(NH4+)>c(Cl-)>c(OH-)>c(H+) D.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
11.室温下,由水电离得到的c(H+)和c(OH-)的乘积为1×10-24的无色溶液中,可能大量共存的离子组是
A.Na+、Fe2+、Br-、Cl- B.AlO2-、K+、NH4+、Na+
C.K+、I-、NO3-、H+ D.K+、S2-、CO32-、OH-
10.有关晶体的下列说法中正确的是
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
9.下列两种气体的分子数一定相等的是
A.质量相等、密度不等的N2和C2H4 B.等体积等密度的CO和C2H4
C.等温等体积的O2和N2 D.等压等体积的N2和CO2
8.巳知某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量存在的离子组是
A.Al3+、CH3C00-、Cl- B.Mg2+、Ba2+、Br-
C.Mg2+、Cl-、I- D.Na+、NH4+、Cl-
7..用pH均为2的盐酸和醋酸溶液,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗盐酸和醋酸溶液的体积分别为Vl和V2,则Vl和V2的关系正确的是
A.V1>V2 B.V1<V2 C.V1=V2 D.V1≤ V2
6.X、Y是元素周期表ⅦA族中的两种元素。下列叙述中能说明X的非金属性比Y强的是
A.X原子的电子层数比Y原子的电子层数多
B.X的氢化物的沸点比Y的氢化物的沸点低
C.X的气态氢化物比Y的气态氢化物稳定
D.Y的单质能将X从NaX的溶液中置换出来
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com