
9.常温下,下列各组离子在指定环境下能大量共存的是
A.pH=l的溶液中:Na+、K+、SO32-、MnO4-
B.pH=7的溶液中:Na+、A13+、Cl-、SO42-
C.pH>12的溶液中:Na+、K+、SO42-、AlO2-
D.pH=0的溶液中:Na+、K+、NO3-、ClO-
8.常温下单质硫主要以S8形式存在。加热时,S8会转化为S6、S4、S2等。当温度达到750℃时,硫蒸汽主要以S2形式存在(占92%)。下列说法正确的是
A.S8转化为S6、S4、S2属于物理变化 B.不论哪种硫分子,完全燃烧都生成SO2
C.常温条件下单质硫为原子晶体 D.把硫单质在空气种加热到750℃即得S2
7.向10mL pH=12的某碱溶液中加入10mL pH=2的盐酸,充分反应后滴入酚酞试液,溶液变红,则此碱一定是 A.弱碱 B.一元强碱 C.多元强碱 D.任何碱
6.在密闭容器中,对已达到化学平衡的反应:2A(g) + B(g)  2C(g);△H<0,其他条件不变,则下列说法中正确的是①升高温度时c(B)/c(C)的比值变小 ②降低温度时,体系内混合气体的平均式量变小 ③加入B后,A的转化率增大 ④加入催化剂,气体总的物质的量不变 ⑤加入C后,则A、B的物质的量均增大
2C(g);△H<0,其他条件不变,则下列说法中正确的是①升高温度时c(B)/c(C)的比值变小 ②降低温度时,体系内混合气体的平均式量变小 ③加入B后,A的转化率增大 ④加入催化剂,气体总的物质的量不变 ⑤加入C后,则A、B的物质的量均增大
A.②③⑤ B.③④⑤ C.①②③⑤ D.全部
5. 某离子晶体中晶体结构最小的重复单元如图:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为
A.B2A B.BA2
C.B7A4 D.B4A7
4. 阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
A.31g 白磷分子(P4)中含有P-P键个数为1.5×6.02×1023
B.48gO2和48gO3所含分子数为3×6.02×1023
C.1.0L 1mol/L氨水中,NH3·H2O的分子数为6.02×1023
 D.20g 重水(D2O)中含有的中子数为8×6.02×1023
D.20g 重水(D2O)中含有的中子数为8×6.02×1023
3.密闭容器中,300℃时将100mL由H2O、CO2、H2和CO组成的混合气体与足量的Na2O2在连续电火花作用下充分反应后,容器内压强只有原来的五分之一,则原混合气体中各组分的体积比不可能是
A.1∶1∶1∶1 B.3∶1∶2∶4 C.1∶3∶5∶1 D.2∶2∶3∶3
2. 已知A2On2-可与B2-反应,B2-被氧化为B单质,A2On2-被还原为A3+,若100mL0.3mol·L-1的A2On2-溶液,与150mL0.6mol·L-1的B2-溶液恰好完全反应,则n的值为
A.5 B.6 C.7 D.8
1.下列热化学方程式中△H的数值能表示可燃物燃烧热的是
A.CO(g)+ O2(g)=CO2(g);△H=-283kJ/mol
O2(g)=CO2(g);△H=-283kJ/mol
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-802.3kJ/mol
C.2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
D.H2(g)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol
26.(12分)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应: N2(g)+3H2(g) 2NH3(g)
2NH3(g)
(1) 若反应进行到某时刻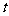 时,
时, =(N2)=13 mol,
=(N2)=13 mol,  (NH3)=6 mol,计算a的值。
(NH3)=6 mol,计算a的值。
(2) 反应达平衡时,混合气体的体积为716.8L(状况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(3) 原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),
 (始):
(始): (平)=________________。
(平)=________________。
(4) 原混合气体中, :
: =___________。
=___________。
(5) 达到平衡时,N2和H2的转化率之比, (N2):
(N2): (H2)_______。
(H2)_______。
(6) 平衡混合气体中, (N2):
(N2): (H2):
(H2): (NH3)_____________。
(NH3)_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com