
1.不会造成水污染的是 ( )
A.工业生产中废气、废液和废渣的排放 B.天然水与空气、岩石和土壤的长期接触
C.城市生活污水的大量排放 D.农业生产中,农药、化肥使用不当
23.(12分)将总物质的量为4mol Na2O2和 Al2(SO4)3混合物投入足量水中,充分反应后生成y mol沉淀(y>0),若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值y=f(x)关系式填写在表内(可填满,也可不填满或补充)并作图。
|
x值 |
y=f(x) |
|
|
|
|
|
|
|
|
|
|
|
|

22. (14分)硝酸是一种重要的化工原料,工业上通常采用氨氧化法制取。某校化学兴趣小组的同学以氯化铵和氢氧化钙为主要原料并设计了下列装置来制硝酸(三氧化二铬为催化剂,加热及夹持装置未画出):
(14分)硝酸是一种重要的化工原料,工业上通常采用氨氧化法制取。某校化学兴趣小组的同学以氯化铵和氢氧化钙为主要原料并设计了下列装置来制硝酸(三氧化二铬为催化剂,加热及夹持装置未画出):
回答下列问题:
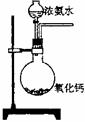
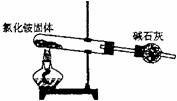
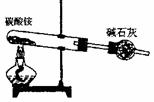
 (1)实验时A中反应的化学方程式是
;A装置(包含药品)不能用下列哪些装置来替代
(填写编号)
(1)实验时A中反应的化学方程式是
;A装置(包含药品)不能用下列哪些装置来替代
(填写编号)
① ② ③ ④
(2)D装置中应填充的物质是 ,该物质的主要作用是 ;
(3)实验结果显示装置F中生成了硝酸,实验前 F装置中的物质是 ;
(4) 若保留上图中黑色粗线框内的装置但去掉通空气的导管B,将C装置中的双孔橡皮塞换成单孔橡皮塞,请你用图示的方法设计一个最简单的实验方案同样完成硝酸的制取(在下面的方框中划出装置图并注明所用药品的名称)。

(5)若要保证氨气全部转化为硝酸,理论上进入C管中的氨气与空气的体积比最多为 。(同温同压下,空气中氧气的体积百分比设为20%)
21. 某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,设计如下方案:
|
|
操
作 |
结
论 |
|
甲 |
火柴梗 |
变黑者为浓硫酸 |
|
乙 |
加入金属铝片 |
产生刺激性气味者为浓硫酸 |
|
丙 |
分别加入到盛水的试管中 |
明显放热者为浓硫酸 |
|
丁 |
用玻璃棒蘸浓氨水靠近酸的瓶口 |
冒白烟者为浓硫酸 |
|
戊 |
加到CuSO4·5H2O晶体中 |
变白者为浓硫酸 |
(1)其中可行的是 。
(2)请给出另外两种鉴别方法
|
|
操
作 |
根据现象做出结论 |
|
A. |
|
|
|
B. |
|
|
20. (12分) 如图:(1)甲、乙、丙是由短周期元素组成的三种单质;(2)组成乙单质的元素的最外层电子数是次外层的2.5倍;(3) C是五核50电子的离子化合物。各物质的关系如下:
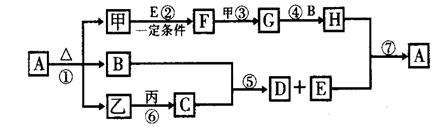
请回答:
(1)各物质的化学式:乙 ,C ,E
(2)写出以下各步化学反应方程式:
①
② .
⑤
19.(8分)有A、B、C、D四种短周期的非金属元素(其单质也可分别用A、B、C、D表示),四种元素的原子序数按B、D、C、A顺序增大,D、C元素在周期表中位置相邻。在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙化合物,C和D化合可得丁。已知乙、丙两个分子中各含有10个电子,并且甲、乙、丙、丁、戊有如下的变化关系:

(1)丙分子的结构式是______________;
用电子式表示乙分子的形成过程 。
(2)写出下列反应的化学方程式:
丙+丁→D + 乙:_____________________________________________
A+丙→D + 甲:_____________________________________________
18.Al和Mg的混合粉末mg滴入盐酸溶液100mL,反应完全后,再向其中滴入1mol/L NaOH溶液,生成的沉淀量和滴入的NaOH的量的关系如图,则下列说法正确的是:
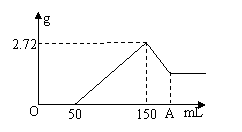 A.A=160
A.A=160
B.m=0.51
C.盐酸的物质的量浓度为1.5mol/L
D.以上说法皆不正确
第II卷(非选择题,共56分)
17.由硫化钠、硫酸钠、亚硫酸钠三种物质组成的混合物中,测得其中含硫的质量分数为25.6%,则混合物中含氧的质量分数为:
A.37.6% B. 36.7% C.51.2% D.无法计算
16.
 同温同压下,当反应物分解了8%时,总体积也增加8%的是
同温同压下,当反应物分解了8%时,总体积也增加8%的是

 A.2NH3(g)
N2(g)+3H2(g) B.2NO(g) N2(g)+O2(g)
A.2NH3(g)
N2(g)+3H2(g) B.2NO(g) N2(g)+O2(g)
C.2N2O5(g) 4NO2(g)+O2(g) D.2NO2(g) 2NO(g)+O2(g)
15.在NH3、HNO3、H2SO4的工业生产中,具有的共同点是
A.使用吸收塔设备 B.使用尾气吸收装置
C.使用H2作原料 D.使用催化剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com