
19.(8分)一般测定样品中成分含量的实验应重重2-3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙两位同学分别设计了如下实验方案:

Ⅰ.甲同学的方案如图所示:
(1)根据甲同学的实验装置图分析,在每次实验过程中所进行的称量操作至少要进行
次;
(2)甲同学重复测定了三次,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能的原因是 (填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.装置外空气的水蒸气和二氧化碳被碱石灰吸收
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收
D.加入稀硫酸的量不足
Ⅱ.乙同学的方案是:称取样品mg,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体n g。
(1)混合物中碳酸钠的质量分数为(用m、n表示) ;
(2)Ca2+、Ba2+都可以使CO32-沉淀完全,但乙同学使用氯化钡溶液而不用氯化钙溶液的原因是
。
16.(8分)某无色溶液,由Na+、Ag+、Ba2+、A13+、[A1(OH)4]-、CO32-、SO42-中的若干种组成。取该溶液进行如下实验:
(A)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
(B)在(A)所得溶液中再加入过量碳酸氢铵固体,有气体生成,同时析出白色沉淀甲;
(C)在(B)所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是
。
(2)一定存在的离子是
。
(3)沉淀乙的成份可能是 ,进一步判断乙的成份的实验方法是
。
15.经测定,某溶液中只含有NH4+、C1-、H+、OH-四种离子。下列说法错误的是 ( )
A.溶液中四种离子之间可能满足:[C1-]>[H+]>[NH4+]>[OH-]
B.若溶液中的溶质是NH4C1和NH3·H2O,则[NH4+]>[C1-]>[NH3·H2O] >[H+]可
能成立
C.若溶液中四种离子满足:[C1-]>[NH4+]>[H+]>[OH-],则溶液中有溶质一定只有
|
D.若溶液中[C1-]=[NH4+],则该溶液一定呈中性
第Ⅱ卷(非选择题,共60分)
14.已知:在25℃时,电离常数Ka(HF)=3.6×10-4mol·L-1,溶度积常数Ksp(CaF2)=1.46×10-10mol3·L-3。现向1L0.2mol·L-1HF溶液中加入1L0.2mol·L-1CaC12溶液,下列说法正确的是 ( )
A.25℃时,0.1mol·L-1HF溶液的pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该混合体系中,
D.该本系中有CaF2沉淀产生
13.甲乙两种醋酸稀溶液,甲的pH=a,乙的pH=a+1。下列判断正确的是 ( )
A.甲中由水电离出来的H+离子的物质的量浓度是乙的0.1倍
B.甲、乙两种溶液的物质的量浓度之间的关系为:c(甲)=10c(乙)
C.中和含有等物质的NaOH溶液,需甲、乙两种酸的体积(V)的关系:10V(甲)>V(乙)
D.甲中c(OH-)为乙中c(OH-)的10倍
12.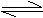 在恒温恒容密闭容器中,建立如下平衡:2A(g)
B(g)。在相同条件下,若再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器中A的质量分数比原平衡时 ( )
在恒温恒容密闭容器中,建立如下平衡:2A(g)
B(g)。在相同条件下,若再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器中A的质量分数比原平衡时 ( )
A.都增大 B.都减少
C.前者增大,后者减小 D.前者减小,后者增大
11.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X,它们的如图所示的转化关系(部分产物及反应条件已略去)。下列判断正确的是 ( )

A.X元素可能为A1 B.X元素可能是金属,也可能是非金属
C.反应①和②互为可逆反应 D.反应①和②一定为氧化还原反应
10.下列说法正确的是 ( )
A.工业用SiO2与焦炭制取单质硅过程中,生成的气体产物是CO
B.硫在空气中燃烧的产物是SO2,在纯净氧气中燃烧的产物是SO3
C.钠在敞口容器中长期存放和在空气中燃烧的产物都是Na2O2
D.镁在空气中和纯净氧气中燃烧的产物都只有MgO
9.根据下列实验事实,得出的结论正确的是 ( )

A.气体 品红溶液褪色
结论:原气体一定是SO2



B.气体 气体 白色沉淀
结论:原气体一定是烃

C.某溶液 冒白雾 白烟
结论:原溶液一定是浓盐酸

D.某无色溶液 紫色
结论:原溶液中一定含有Fe3+
8.表示下列变化的化学用语,正确的是 ( )
A.钢铁吸氧府蚀的正极反应式:O2+2H2O+4e- →4OH-
|
 C.碳酸氢钠溶液显碱性:HCO3-+H2O CO2-3+H3O+
C.碳酸氢钠溶液显碱性:HCO3-+H2O CO2-3+H3O+
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com