
13.同温、同压下,等体积的两容器内分别充满由有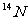 、
、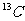 、
、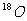 三种原子构成的一氧化氮和一氧化碳,下列说法正确的是
三种原子构成的一氧化氮和一氧化碳,下列说法正确的是
A.含有相同数目的中子、原子和分子
B.含有相同的分子数和电子数
c.含有相同的质子数和中子数
D.所含分子数和质量数均不相等
12.2005年诺贝尔化学奖获得者施罗克等人发现,金属钼的卡宾化合物可以作为非常有效
的烯烃复分解催化剂。工业上冶炼钼的化学原理为:
①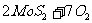


②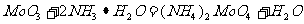
③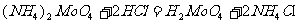
④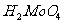

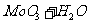
⑤用还原剂将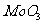 还原成金属钼
还原成金属钼
则下列说法正确的是
A.煅烧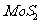 产生的尾气可以直接排空
产生的尾气可以直接排空
B.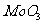 是金属氧化物,也是碱性氧化物
是金属氧化物,也是碱性氧化物
C.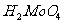 是一种强酸
是一种强酸
D.用铝热法制得1mol钼所消耗铝的质量为54g
11.下列为某同学根据中学化学教材中数据所进行的判断,其中错误的是
A.根据溶解度数据,判断长时间煮沸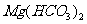 溶液所得的沉淀是
溶液所得的沉淀是 还是
还是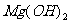
B.根据反应热数据,判断不同反应的反应速率大小
C.根据沸点数据,判断能否用分馏的方法分离一些液体混合物
D.根据相对分子质量数据,判断组成和结构相似的物质的熔点和沸点的高低
10.下列说法中正确的是
A.硅是人类将太阳能转化为电能的常用材料
B.提倡使用乙醇汽油主要是为了提高汽油的燃烧效率
C.赤潮、潮汐、酸雨、臭氧空洞都是与环境污染有关的现象
D.在松花江污染事件中,使用活性炭减少污染是因为活性炭与硝基苯发生了化学反应
9.2006年10月4日诺贝尔化学奖授予美国科学家罗杰·科恩伯格,以表彰其在分子层面上提供真核转录实际过程,揭示细胞如何依据遗传基因所提供的信息生成蛋白质,有助于探寻治疗癌症、心脏病和各种炎症的新方法。下列有关说法不正确的是
A.化学家通过对分子和原子的分析、控制和过程模拟解决了许多自然之谜
B.蛋白质溶液是一种胶体
C.向蛋白质溶液中加入硫酸钠溶液会发生变性
D.蛋白质溶液可以发生丁达尔现象
22.(9分)A、B、C、D、E、是五种常见的单质,A、B、C、D在常温下均为气体,其中,C是空气中含量最多的,D是所有气体中密度最小的;D能分别跟A、B、C在一定条件下化合,生成化合物X、Y、Z;A与B、C均不能直接化合。有关转化关系如图所示(反应条件均已略去)。

回答下列问题:
(1)A的化学式为 ,G的化学式为 ;
(2) 反应①的化学方程式为 ;
(3)过量E与N的稀溶液反应的离子方程式为 ;
(4)若将2.8g单质E与50mL 3mol·L-1N的溶液反应,生成溶液中溶质的成分是 ,其中物质的量之比为 。
21.(9分)在一固定容积的密闭容器中,进行如下化学反应:
 CO2(g)+H2(g)
CO(g)+H2O(g);△H=QkJ·mol-1
CO2(g)+H2(g)
CO(g)+H2O(g);△H=QkJ·mol-1
其化学平衡常数K和温度t的关系如下:
|
t℃ |
700 |
800 |
850 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
请回答:
(1)上述反应中Q 0(选填“>”或 “<”);
(2)参判断该反应已达到化学平衡状态的依据是 。
a.容器中压强不变 b.反应热△H不变
c.v正(H2)=v逆(CO) d.CO2的质量分数不变
 (3)温度为850℃时,可逆反应CO2(g)+H2(g) CO2(g)+H2(g)在固定容积的密闭容器中进行,容器内各物质的浓度变化如下表:
(3)温度为850℃时,可逆反应CO2(g)+H2(g) CO2(g)+H2(g)在固定容积的密闭容器中进行,容器内各物质的浓度变化如下表:
|
时间(min) |
CO |
H2O |
CO2 |
H2O |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
C1 |
C2 |
C3 |
C3 |
|
4 |
C1 |
C2 |
C3 |
C3 |
|
5 |
0.116 |
0.216 |
0.084 |
|
|
6 |
0.096 |
0.266 |
0.104 |
|
①计算:3min时(CO浓度)c1= mol/L,H2O(g)的转化率为 。
②反应在4min-5min之间,平衡向逆方移动,可能的原因是 (单选),表中5min-6min之间数值发生变化,可能是原因是 (单选)。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
20.(8分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A与D同主族,B、C同周期;B原子最外层电子数比其次外层电子数多2;B、A两元素的核电荷数之差等于它们的原子最外层电子数之和;E元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E形成的化合物甲、乙、丙、丁、戊的组成如下表所示:
|
化合物 |
甲 |
乙 |
丙 |
丁 |
戊 |
|
分子式 |
A2C |
A2C2 |
B2A2 |
D2C2 |
DE |
回答下列问题:
(1)化合物丁中存在的化学键类型是 ;
(2)向含有0.2mol乙的水溶液中加入少量MnO2,使乙完全反应,发生转移的电子数为
NA(NA代表阿伏加德罗常数的值);
(3)用铁作阴极、石墨作阳极,电解甲、戊的混合物,电解反应的离子方程式为:
;
(4)2.0g丙完全燃烧,生成液态甲和B的气态氧化物,放出99.9kJ的热量,此燃烧反应的热化学方程式为 。
19.(6分)青霉素是常用抗生素,其结构可表示为:
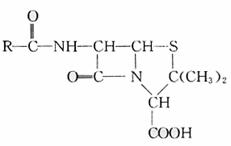
(不同品种青霉素的结构式中,R-为不同的基团)。
(1)阿莫西林是一种常用青霉素,它是结构式中R-为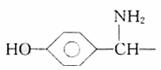 。
。
①阿莫西林分子中显酸性的官能团是 (填名称);
②下列关于阿莫西林的说法中,正确的是 (填标号)。
A.是高分子化合物 B.属于芳香烃
C.分子式为C16H19O5N3S D.可与浓溴水反应生成白色沉淀
(2)青霉素G(C16H18O4N2S)是一种天然青霉素,其结构式中的R一为含苯环的烃基,R-的结构可能有 种。
18.(12分)某链状聚酯G(聚合度为n)常被用作外科手术缝合线和骨科手术固定膜,手术后能在定期内被人体分解吸收。其合成路线如下:
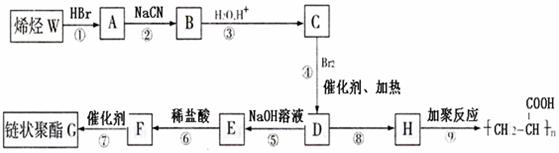
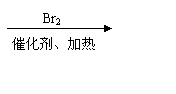
已知:RCH2COOH R-CH-COOH,试回答
|
Br
(1)写出结构简式:W
G ;
(2)写出反应类型:④
⑦ ;
(3)反应⑧的条件是 ;
(4)写下理列反应方程式:
②
⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com