
6.在下列各氧化还原反应中,水既不作氧化剂,也不作还原剂的是
|
C.2Na+2H2O==2NaOH+H2↑ D.Cl2+H2O==HCl+HClO
5.下列含有非极性键的共价化合物是
A.HCl B.Na2O2 C.C2H2 D.CH4
4.实现下列各组物质的变化时,需克服的作用力完全相同的是
A.硫磺和氢氧化钠的熔化 B.二氧化硅和生石灰的熔化
C.碘和萘的升华 D.氯化钠和铁的熔化
3.下列物质属于弱电解质的是
A.氯化铝 B.铜 C.酒精 D.水
2.下列化学式既能表示物质的组成,又能表示物质的一个分子的是
A.NaOH B.C C.SiO2 D.CO2
1.闪电时空气中有臭氧生成,下列说法正确的是
A.O2和O3互为同位素 B.O2比O3稳定
C.等体积的O2和O3具有相同的质子数D.O2与O3的相互转变是物理变化
25.(8分)室温下,向50mL Ba(OH)2溶液中滴加0.5mol/L的NaHSO4溶液。当NaHSO4溶液滴加到20mL后沉淀质量就不再增加了。试计算当NaHSO4溶液滴加到50mL时:(忽略溶液混合前后体积变化的影响)
求:(1)产生沉淀的质量
(2)溶液的pH值(lg5=0.7)
24.(12分)为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。

(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。其中第一步实验操作为: 。从装置的设计看,确定E中空气已被赶尽的实验现象是:______________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 。有人认为E中收集到的可能是H2而不是NO,如何证明? 。
(3)实验过程中,发现在未鼓入空气的情况下,E中就产生红棕色。有人认为是由装置E部分设计不当造成的。你认为装置应改进的地方是 。
(4)装置A中将铜丝设计成能上下移动的目的是 。
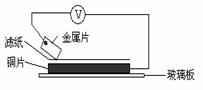
23.(10分)将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如右图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下:
|
金属 |
电子流动方向 |
 电压(V) 电压(V) |
|
A |
A→Cu |
+ 0. 78 |
|
B |
Cu→B |
–0.15 |
|
C |
C→Cu |
+ 1.35 |
|
D |
D→Cu |
+0.30 |
已知:构成两电极的金属其金属活泼性相差越大,电压表的读数越大。
请依据表中数据判断:
(1) (填字母)金属可能是最强的还原剂; (填字母)金属不能从硫酸
铜溶液中置换出铜。
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到的蓝色沉淀析出
的是 (填字母)金属。其对应的原电池的电极反应式为:负极
,正极 。
|

(1)若气体P就是单质Y,则X单质是 ,Y单质是 ,化合物Q电子式
为 。
(2)若气体P有臭鸡蛋气味,化合物Q是可溶于强碱溶液的白色沉淀,则X单质是 ,Y单质是 ,化合物Q溶于强碱溶液的离子方程式为 。
(3)若气体P能使湿润的红色石蕊试纸变蓝,化合物Q是可溶于强酸的白色沉淀,则X单质是 ,Y单质是 ,化合物Z和水反应的化学方程式为 。
22.(8分)发射“神舟”飞船的火箭用肼(N2H4)作燃料,N2H4与NH3有相似的化学性质。
(1)写出肼与盐酸反应的离子方程式 。
(2)用拉席希法制备肼,是将NaClO和NH3按物质的量之比1:2反应生成肼,试写出该反应的化学方程式 。该反应中 是氧化产物。
(3)发射火箭时肼(N2H4)为燃料,NO2作氧化剂,两者反应生成氮气和气态水。已
知4gN2H4(g)在上述反应中放出71KJ的热量,请写出该反应的热化学方程式
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com